Introducción
La región de Asia y el Pacífico se ha vuelto atractiva para la realización de ensayos clínicos porque es fácil adherirse a la normativa, el costo de los estudios es bajo, hay una población creciente de pacientes y establecimientos de salud de prestigio que cuentan con centros de investigación. Por ejemplo, las agencias reguladoras en China están trabajando para mejorar los procesos de los ensayos clínicos, a la vez que aceleran el proceso general de revisión y aprobación [1]
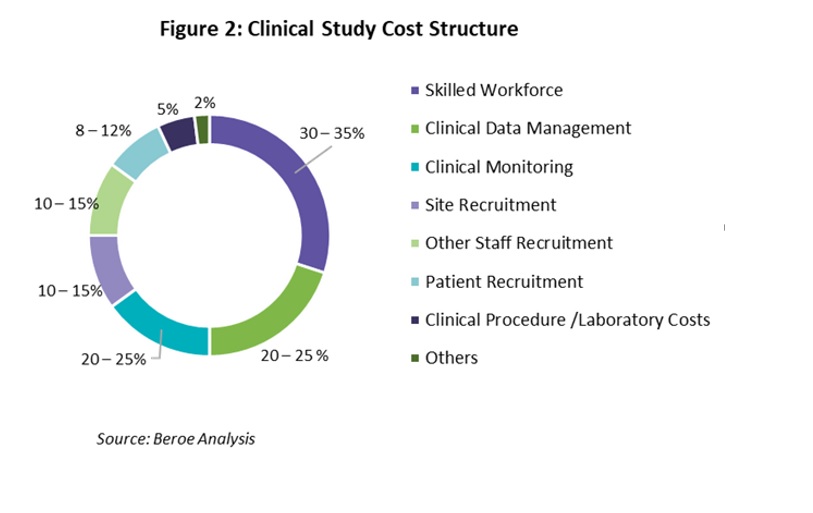
El costo del personal que realiza los ensayos clínicos representa alrededor del 30 o 35% del costo total del ensayo. Esto hace que el salario de un FTE* (full time equivalent, empleado de tiempo completo) para la investigación clínica sea un parámetro clave a considerar. Estos costos son generalmente más altos en los mercados desarrollados que en la región de Asia y el Pacífico, por lo que esta última se está convirtiendo en un lugar importante para realizar ensayos clínicos. Además, en todas las áreas y fases terapéuticas el costo por paciente es mucho menor en los países asiáticos que en los mercados desarrollados.
Descripción general del mercado de las CROs en Asia y el Pacífico
En 2021, el mercado de las CROs en Asia y el Pacífico está valorado en aproximadamente US$7.600 millones y se prevé que alcance los US$11.900 millones en 2025. Entre 2017 y 2025, gracias a la facilidad en recibir la aprobación regulatoria, el bajo costo de los salarios FTEs, la disponibilidad de un gran número de pacientes y la presencia proveedores, se espera que la región de Asia y el Pacífico experimente una tasa de crecimiento anual compuesta (tasa de crecimiento CAGR**) del 12%.
El impacto de COVID-19 impulsó una revolución digital que incluyó el análisis de las grandes bases de datos (data mining en inglés), el uso de inteligencia artificial y tecnologías que utilizan grandes bases de datos (Big Data) que promueven el diagnóstico basado en datos y la salud digital [2]. Esto ha provocado que alrededor del 65% de las actividades de las empresas farmacéuticas se subcontraten a CROs, una cifra que se espera que en el futuro alcance el 75%. A la vez, la demanda de productos farmacéuticos innovadores ha presionado a las empresas farmacéuticas a aumentar el gasto en I + D para poder ofrecer estos nuevos productos mientras controlan los costes [3].
Dado que uno de los componentes importantes del costo de los ensayos clínicos es el pago a la fuerza laboral, como se muestra en la Figura a continuación, el hecho de que los salarios de un FTE sean más bajos en Asia y el Pacífico la convierten en una región deseable para realizar ensayos clínicos. Sin embargo, los salarios no son los mismos en toda la región de Asia y el Pacífico. Australia y Japón tienen los salarios más altos, seguidos de China, Hong Kong e India. Malasia y Filipinas tienen los salarios más bajos.
Además, el cambio hacia la realización de ensayos clínicos en países en desarrollo ha ido generado la experiencia necesaria para hacer ensayos globales en Asia. Personal del estudio global entrena al personal calificado de esos países, y se están adquiriendo conocimientos sobre las buenas prácticas clínicas de la Conferencia Internacional sobre Armonización (ICH, por sus siglas en inglés) en toda la región. El personal interactúa a nivel internacional, lo que significa que pueden realizar ensayos clínicos y utilizar los resultados para las presentaciones a la EMA y FDA. Aunque en el pasado algunas empresas detectaron problemas de calidad y un comportamiento ético cuestionable, con la implantación de regulaciones estrictas y de supervisión esto está cambiando en los países en desarrollo. Por ejemplo, Corea del Sur adoptó ICH-GCP en 2001, reemplazando su legislación local. Además, las notificaciones oficiales que emite la FDA tras las inspecciones han disminuido en la mayor parte de los países de Asia y el Pacífico. Esto se traduce en un aumento de la calidad de los datos provenientes de estos sitios [4].
Tendencias en la oferta de mercado
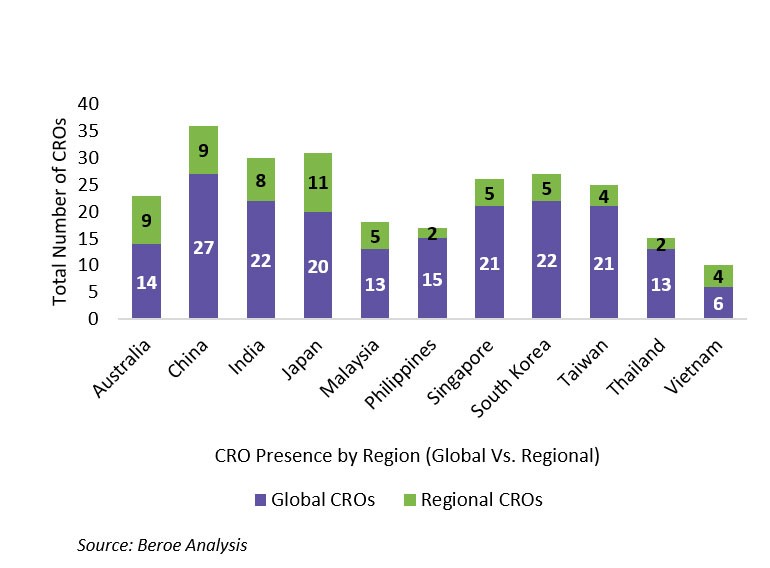
Las CROs globales como Covance, Icon, IQVIA, Paraxel, PPD, PRA, etc. tienen una presencia muy fuerte en Asia y el Pacífico, y sus ofertas de servicios son muy parecidas. Las CROs regionales tienen una presencia igualmente fuerte, debido a su experiencia local. También se estima que los costos de operación de los actores regionales son entre un 20 y un 40% más baratos que los globales, ya que tienen gastos generales más bajos y estructuralmente son menos complejos debido a la toma local de decisiones; por tanto, tienen mayor eficiencia. Los actores regionales clave como WuXi Apptec, Syngene, CMIC Group, TigerMed y Lambda CRO tienen buena participación en el mercado regional y se han asociado con las grandes compañías farmacéuticas para realizar ensayos clínicos.
Presencia de CROs por region (Global vs Regional)
Conclusión
Los menores costos en salarios, transporte y tarifas regulatorias permiten ahorrar alrededor del 30 al 40% del costo de los ensayos que se realizan en la región de Asia-Pacífico en comparación con el precio en los mercados desarrollados. Los sistemas de atención médica de Singapur, Taiwán, Corea y Hong Kong son avanzados, y muchos médicos de estos países se han capacitado en EE UU o Europa. La pandemia de COVID-19 ha logrado que se hagan inversiones para utilizar las plataformas digitales y evitar interrupciones en los ensayos clínicos, permitiendo que los médicos monitoreen a los pacientes de manera remota y eficiente. Con una oferta de mercado favorable y una fuerte presencia de CROs globales y regionales con experiencia local, las compañías farmacéuticas consideran que la región de Asia-Pacífico es un mercado atractivo para la realización de ensayos clínicos.
Referencias
Notas de los editores del Boletín: