Políticas
América Latina
Comunicado de las organizaciones miembros del Comité de Veeduría y Cooperación en Salud (CVCS) con respecto al estado actual del proceso de Declaratoria de Interés Público con fines de licencia obligatoria del medicamento imatinib
Bogotá, abril 20 de 2016
El Ministerio de Salud y Protección Social ha divulgado en los últimos días por distintos medios la propuesta presentada por el Ministro de Salud, Doctor Alejandro Gaviria Uribe, a la compañía farmacéutica multinacional Novartis, productora del medicamento Glivec® (imatinib), en desarrollo de la recomendación contenida en el informe del Comité Técnico competente, para la reducción de su precio a niveles de competencia simulada, a fin de asegurar que resulte adecuado para la sostenibilidad del sistema de salud y no afecte la prestación de otros servicios esenciales a la población [1].
Por su parte, los defensores de los intereses comerciales de la multinacional, entre ellos el propio Novartis [2], PhRMA, el gremio de las multinacionales farmacéuticas en Estados Unidos [3], AFIDRO, gremio nacional de las multinacionales farmacéuticas [4], y la Superintendencia Delegada para la Propiedad Industrial de la Superintendencia de Industria y Comercio [5], han hecho en diversos escenarios, ya sea en directa alusión a este proceso en curso o de manera indirecta, afirmaciones que bien pueden interpretarse como un rechazo de la solicitud de la declaratoria de interés público del imatinib, del mecanismo de las licencias obligatorias, del informe de recomendación del citado Comité Técnico y de la mencionada propuesta del Ministro de Salud, todo con miras a lograr que en el corto plazo Novartis pueda mantener los altos niveles de precio, ventas y utilidades que registra actualmente en el país gracias al Glivec®, y en el mediano y largo plazo que siga siendo aplazada la utilización del mecanismo de las licencias obligatorias como herramienta legítima y efectiva a favor de la salud pública.
Sobre el particular, las organizaciones firmantes del presente comunicado, en cumplimiento de su compromiso con la promoción y defensa del derecho fundamental a la salud y a los medicamentos necesarios para la salud y la vida, presentamos las siguientes declaraciones:
1. Felicitamos al Ministerio de Salud y Protección Social por la transparencia con la que ha impulsado el actual proceso, sentando un valioso precedente sobre la gobernanza, la priorización del derecho a la salud sobre los intereses comerciales y los mecanismos a disposición de los Estados para ejercer su soberanía en el campo de la salud.
2. Respetuosamente nos apartamos de la propuesta presentada por el Ministro de Salud a Novartis ($140 por mg), pues si bien obedece a un juicioso análisis económico y estadístico, se aleja conceptualmente de lo que se entendería como “competencia simulada” al estar muy por encima de los precios que se lograrían con la expedición de una licencia obligatoria (ver Anexo 1).
3. Las condiciones para la declaración de interés público del imatinib y el consecuente otorgamiento de licencia obligatoria sí existen. El otorgamiento de licencias obligatorias es un derecho consagrado en el ordenamiento jurídico internacional vigente, ejercible siempre que haya razones de salud pública que lo justifican, como conjurar una emergencia sanitaria o poner remedio a prácticas anticompetitivas, por ejemplo la fijación de precios inaccesibles (ver Anexo 2).
4. Considerando el actual proceso de declaración de interés público como extremadamente contencioso, insistimos en la importancia de que continúe por las vías legales y que en caso de que prospere la declaración de interés público del imatinib, como consideramos que es lo procedente, se den las garantías desde la Superintendencia de Industria y Comercio de un proceso administrativo alrededor de la licencia obligatoria que cumpla los principios de publicidad, transparencia, eficacia y celeridad.
5. En este contexto y teniendo en cuenta que la misión de la Superintendencia de Industria y Comercio es salvaguardar los derechos de los consumidores, proteger la libre y sana competencia y actuar como la autoridad nacional de la propiedad industrial, encontramos completamente alejado del interés público que sus funcionarios tomen partido en defensa de la compañía multinacional involucrada en el actual proceso, máxime si se trata de aquellos servidores públicos en cuyas manos puede llegar a estar la definición final del caso.
6. Instamos al Ministro de Salud y Protección Social a proceder sin más dilaciones a declarar el interés público del imatinib, por el beneficio que esto representará tanto en términos de acceso a este medicamento, esencial para el tratamiento de la leucemia y otros tipos de cáncer, y de sostenibilidad financiera del sistema de salud, como por el precedente histórico de proteger el derecho fundamental a la salud del abuso de intereses comerciales privados que apelan al miedo, las amenazas y las dudas en procura de que el Estado deje de hacer aquello que se sabe es lo correcto y que es posible.
Monseñor Fabián Marulanda
Conferencia Episcopal de Colombia
Sergio Isaza Villa
Federación Médica Colombiana
Germán Holguín Zamorano
Misión Salud
Francisco Rossi Buenaventura
Fundación Ifarma
José Julián López Gutiérrez
Centro de Información de Medicamentos de la Universidad Nacional de Colombia – CIMUN
Oscar Andia Salazar
Observatorio del Medicamento de la Federación Médica Colombiana – OBSERVAMED
Jennifer M. Bueno Rocha
Comité de Veeduría y Cooperación en Salud
Anexo 1
2. Respetuosamente nos apartamos de la propuesta presentada por el Ministro de Salud a Novartis ($140 por mg), pues si bien obedece a un juicioso análisis económico y estadístico, se aleja conceptualmente de lo que se entendería como “competencia simulada” al estar muy por encima de los precios que se lograrían con la expedición de una licencia obligatoria.
En efecto, según cálculos de OBSERVAMED, basados en reportes del SISMED, mientras el precio del Glivec® es de $330/mg, los de otros productos oscilan entre $55 y $84/mg, para un promedio cercano a $70/mg. [6].
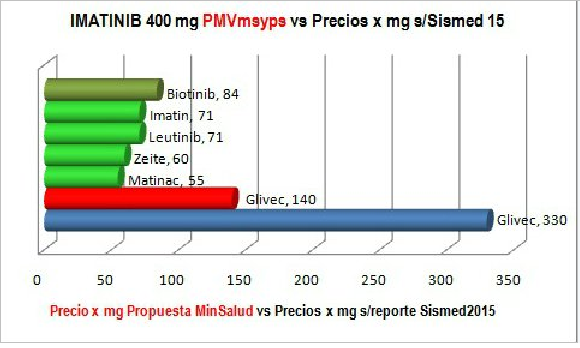
En otras palabras, la propuesta del Ministro equivale al doble de lo que podría considerarse “competencia simulada” y supera ampliamente el precio que podría alcanzarse a través de una licencia obligatoria, con los efectos consiguientes sobre el acceso al medicamento en cuestión, la salud de quienes lo requieren para tratar la enfermedad y prolongar la vida, y la posibilidad de que el sistema ahorre miles de millones de pesos, utilizables en la satisfacción de otras prioridades sanitarias.
En consecuencia, en caso de llegarse a una negociación entre el Ministro y Novartis con base en la propuesta de aquel, las organizaciones firmantes nos veríamos forzadas a insistir en la Declaratoria de Interés Público y la concesión de la licencia Obligatoria [6].
Anexo 2
3. Las condiciones para la declaración de interés público del imatinib y el consecuente otorgamiento de licencia obligatoria sí existen. El otorgamiento de licencias obligatorias es un derecho consagrado en el ordenamiento jurídico internacional vigente, ejercible siempre que haya razones de salud pública que lo justifican, como conjurar una emergencia sanitaria o poner remedio a prácticas anticompetitivas, por ejemplo la fijación de precios inaccesibles.
No es cierto que, como lo sostienen los defensores de los intereses comerciales de Novartis, la licencia obligatoria sea un instrumento utilizable únicamente como medida excepcional en casos extremos. Ni el Acuerdo de los ADPIC ni la Declaración de Doha ni la Decisión 486 del 2000, que son los instrumentos que reglamentan este derecho, contienen disposiciones con tal alcance. Si existieran, es claro que las citarían los voceros de Novartis, lo cual no ha ocurrido ni podría ocurrir.
Por el contrario, la Declaración de Doha, después de reconocer los efectos negativos de la propiedad intelectual sobre los precios y el acceso (puntos 1 a 4), reafirma el “derecho de los miembros de la OMC de utilizar, al máximo, las disposiciones del ADPIC que prevén flexibilidades a este efecto” (punto 4, segundo párrafo) y reconoce que estas flexibilidades incluyen el “derecho de conceder licencias obligatorias y la libertad de determinar las bases sobre las cuales se conceden” (punto 5b).
De esta manera el ADPIC y la Declaración de Doha convierten las licencias obligatorias en el principal instrumento con el que cuentan los gobiernos para “limitar los derechos exclusivos del titular de la patente cuando sea necesario para alcanzar ciertos objetivos de la política pública, en particular para asegurar la disponibilidad de fuentes alternativas de suministro de medicamentos a precios bajos”[7].
“El derecho del Estado de conceder licencias obligatorias se deriva de su obligación de proteger el derecho a la salud y a los medicamentos de los efectos dañinos de… las patentes farmacéuticas, mediante la adopción de medidas que posibiliten el cumplimiento de su deber-obligación” [8].
Es un derecho de los pueblos, emanado del mismo instrumento de derecho internacional que los derechos de propiedad intelectual. Con una diferencia: que el derecho a conceder licencias obligatorias, por estar vinculado al derecho fundamental a la salud y la vida, es de categoría superior y prima sobre los derechos de propiedad intelectual.
Finalmente, ninguno de los tratados comerciales suscritos por Colombia, incluidos el negociado con la Asociación Europea de Libre Comercio (AELC), de la que forma parte Suiza, país sede de Novartis, y el Convenio entre la República de Colombia y la Confederación Suiza sobre la Promoción y la Protección Recíproca de Inversiones, contienen limitaciones al uso de las licencias obligatorias. Si las hubiera, es obvio que las citarían los defensores de Novartis. Por el contrario, es común que los tratados reconozcan la importancia de la Declaración de Doha y comprometan a las partes a asegurar que la interpretación de los derechos y obligaciones asumidos bajo el Capítulo de Propiedad Intelectual serán consecuentes con dicha Declaración, a fin de que puedan suministrar medicamentos a precios accesibles en desarrollo de sus programas nacionales de salud pública.
En conclusión, cuando el Gobierno colombiano declare el interés público del imatinib y conceda la respectiva licencia obligatoria, lo hará en cumplimiento de su obligación de respetar, proteger y cumplir el derecho fundamental a la salud, y en ejercicio del derecho soberano de utilizar plenamente las flexibilidades previstas en el Acuerdo ADPIC para asegurar el acceso a los medicamentos necesarios para el bienestar de las personas. Porque la salud y la vida del pueblo colombiano están por encima de los intereses comerciales de las multinacionales farmacéuticas, por poderosas e influyentes que ellas sean.
Referencias