Os anúncios farmacêuticos nos Estados Unidos são irritantes. Absurdos. E quase exclusivamente americanos.
Na verdade, apenas um outro país de alta renda em todo o mundo — a Nova Zelândia — permite que os laboratórios de medicamentos de prescrição anunciem diretamente aos consumidores. Todos os outros decidiram que as desvantagens não valem a pena. Então, por que os EUA não os proibiram?
Desde o início, RFK Jr. definiu a eliminação dos anúncios farmacêuticos como um de seus objetivos. E, acredite ou não, concordo com ele nessa questão. (Uau!) Mas será que o governo pode realmente tomar providências? Eles acham que sim. Ontem, um novo memorando executivo e um comunicado à imprensa da Administração de Alimentos e Medicamentos (FDA) fizeram uma solicitação para intensificar a fiscalização contra os anúncios de medicamentos [1,2].
Aqui vão respostas para as 9 perguntas principais.
Mas, na década de 1980, a FDA decidiu que isso não era exatamente verdade. A agência concluiu que os anúncios de medicamentos eram legais, desde que incluíssem um “breve resumo” do rótulo do medicamento aprovado pela FDA. Foi então que os anúncios em revistas sofisticadas decolaram — fotos grandes e chamativas em uma página, com letras minúsculas resumindo os riscos na página seguinte.
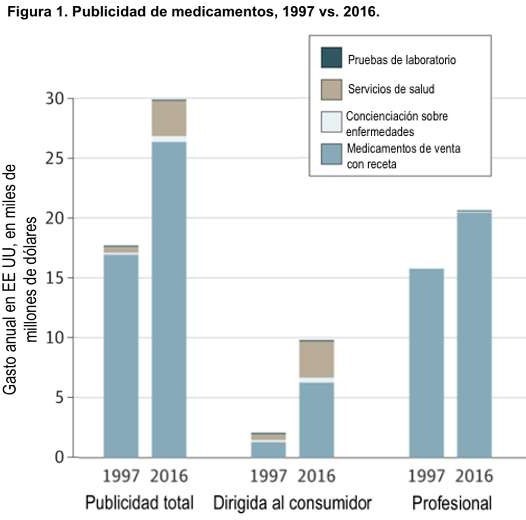
Em 1997, a FDA fez outra mudança fundamental: na TV e no rádio, os fabricantes de medicamentos não precisavam mais do resumo completo. Em vez disso, eles podiam fornecer uma “declaração importante” dos principais riscos. Esse foi o momento em que a era moderna dos comerciais farmacêuticos começou.
Mas os anúncios influenciam os medicamentos que os pacientes pedem, e esses tendem a ser os mais caros.
Os fabricantes de genéricos raramente anunciam porque enfrentam o que os economistas chamam de problema do “carona” (free-rider). Várias empresas fabricam o mesmo medicamento genérico. Se você pedir um genérico ao seu médico, a farmácia lhe dará a versão que estiver em estoque, não uma marca específica. Isso significa que um anúncio de uma empresa de genéricos também pode impulsionar as vendas de seus concorrentes. Por que se dar ao trabalho?
Como resultado, quase todos os anúncios de medicamentos são de medicamentos de marca caros. Isso significa que os pacientes que respondem aos anúncios muitas vezes acabam pagando por esses medicamentos caros, mesmo quando existe um genérico mais barato e igualmente eficaz ou até mesmo um tratamento sem medicamentos.
Outro estudo descobriu que menos de um terço dos medicamentos mais comuns apresentados em anúncios televisivos direcionados ao consumidor foram classificados como tendo alto valor agregado para os pacientes [6].
Além disso, os anúncios de medicamentos devem apresentar “equilíbrio justo” (fair balance), o que significa que os aspectos positivos e negativos precisam ser ambos apresentados. Na prática, isso geralmente quer dizer que a primeira metade do comercial mostra pessoas se divertindo na praia, enquanto a segunda metade é uma enumeração vertiginosa de advertências.
Figura retirada de Medical Marketing in the United States, 1997-2016 (Marketing médico nos Estados Unidos, 1997-2016) na JAMA. Fonte [5].
O Escritório de Promoção de Medicamentos de Prescrição (OPDP) da FDA deve garantir que os anúncios sejam precisos, não enganosos e razoavelmente equilibrados. Mas aqui está o problema: as empresas não precisam enviar os anúncios para aprovação antes de exibi-los. Quando o OPDP encontra anúncios problemáticos, geralmente é meses depois de eles terem sido divulgados.
E o que é considerado “enganoso” nem sempre é claro. Veja o caso de um anúncio que promove um novo medicamento para dormir que ajuda as pessoas a “adormecer rapidamente” [7]. Isso parece impressionante até você descobrir que, no estudo que levou à aprovação do medicamento pela FDA, os pacientes que tomaram o medicamento adormeceram em 30 minutos, enquanto as pessoas que tomaram placebo adormeceram em 45 minutos. Não é uma grande diferença. O anúncio é tecnicamente enganoso? É difícil dizer.
A psicologia complica ainda mais as coisas. Estudos mostram que, quando os riscos dos medicamentos são lidos em voz alta enquanto imagens calmantes são exibidas ao fundo, os espectadores se distraem das informações sérias [8]. O anúncio cumpre as regras, mas o impacto sobre os pacientes é outra história.
Por um lado, os anúncios de medicamentos aumentam a prescrição dos medicamentos apresentados. É possível imaginar um caso em que isso seja bom. Pacientes que, de outra forma, poderiam sofrer em silêncio, por exemplo, com disfunção erétil ou depressão, podem ser incentivados a iniciar conversas com seus médicos. Em teoria, os anúncios podem empoderar as pessoas a procurar tratamento para condições estigmatizadas.
Por outro lado, os anúncios podem levar à “prescrição excessiva”. Se um paciente entra no consultório médico e pede um medicamento pelo nome, estudos mostram que é mais provável que ele o receba, mesmo que uma abordagem diferente pudesse ter sido melhor [9]. Isso levantou preocupações sobre os anúncios incentivarem o uso desnecessário ou inadequado, especialmente para condições como TDAH em adultos, olhos secos ou transtorno de adaptação.
A verdade é que os anúncios de medicamentos são uma faca de dois gumes. Eles podem abrir portas para o cuidado, mas, na maioria das vezes, incentivam prescrições caras e até mesmo desnecessárias.
A maior delas é a Primeira Emenda. A proibição dos anúncios de medicamentos teria que ser defendida na Justiça, já que as empresas farmacêuticas entrariam imediatamente com uma ação para revogar a proibição. Mas a Suprema Corte interpretou a proteção da liberdade de expressão da Primeira Emenda como abrangendo entidades comerciais, mesmo que as empresas não sejam pessoas. Infelizmente, é difícil imaginar uma mudança na perspectiva atual dos tribunais sobre a liberdade de expressão comercial, a menos que haja uma emenda constitucional que esclareça que as empresas não são pessoas e não merecem proteções semelhantes à liberdade de expressão.
Portanto, se não for uma proibição — e na ausência de um acordo voluntário dos laboratórios para interromper a publicidade —, o governo poderia tentar regulamentar os anúncios de medicamentos de forma mais rigorosa. Por exemplo, a FDA poderia criar regras sobre seu conteúdo ou onde e quando eles podem ser exibidos. Os anúncios online, em particular, podem ter características que os tornam propensos a interpretações erradas — por exemplo, como as informações sobre riscos são exibidas ou como elementos de design que distraem (como vídeos com reprodução automática ou pop-ups) podem afetar a compreensão. A FDA poderia tentar identificar tais situações e estabelecer regras para lidar com elas. O Congresso também poderia fornecer mais recursos e autoridade à FDA para identificar rapidamente anúncios problemáticos e removê-los de circulação.
A indústria farmacêutica tem a organização de lobby mais poderosa e com mais recursos em Washington D.C. Ela historicamente se opôs a quaisquer esforços que restringissem a capacidade dos fabricantes de anunciar amplamente porque, como observado acima, os anúncios de medicamentos ajudam os fabricantes de marcas famosas a ganhar dinheiro. A indústria forneceu fundos substanciais ao longo dos anos a muitos legisladores e ajudou a eleger presidentes que definiram a agenda e o financiamento da FDA.
As principais medidas incluídas na diretiva são:
O impacto dessas medidas provavelmente será limitado. As cartas de advertência quase sempre resultam apenas na retirada ou ajuste do anúncio pela empresa, sem multas ou penalidades adicionais — muitas vezes meses depois que o anúncio já foi amplamente divulgado. Com os recentes cortes de pessoal e orçamento na FDA, também será difícil manter uma supervisão consistente e agressiva das redes sociais. A diretiva nem sequer tenta fornecer detalhes sobre a chamada supervisão ampliada, como diretrizes essenciais sobre o que deve ou não ser permitido na publicidade de medicamentos nas redes sociais. Detalhes desse tipo se fizeram necessários há muitos anos (e ainda são necessários)!
Conclusão
Os anúncios de medicamentos de prescrição são uma forma limitada e inerentemente problemática de informar as pessoas sobre medicamentos de prescrição. Precisamos fazer um trabalho muito melhor para capacitar os pacientes a obterem o cuidado médico de que precisam e para educá-los sobre os verdadeiros benefícios e riscos dos medicamentos de prescrição de forma imparcial.
Se isso vai mudar ou não, dependerá não apenas de um governo, mas de como nós, como país, decidimos equilibrar o poder corporativo, a propaganda comercial e a saúde de nossos cidadãos.
Referências