Investigaciones
Subvenciones de patentes farmacéuticas en la India: cómo han fracasado nuestras salvaguardas contra la perennización y por qué se debe reformar el sistema (Pharmaceutical patent grants in India: How our safeguards against evergreening have failed, and why the system must be reformed)
Dr. Feroz Ali, Dr. Sudarsan Rajagopal, Dr. Venkata S. Raman & Roshan John
Creative Commons, April 2018
Una publicación de la Universidad de Azim Premji
https://www.accessibsa.org/media/2018/04/Pharmaceutical-Patent-Grants-in-India.pdf
Traducido por Salud y Fármacos
Resumen ejecutivo
Introducción
Este informe identifica, en una cohorte de 2293 patentes otorgadas entre 2009 y 2016, las patentes de productos farmacéuticos que posiblemente fueron otorgadas en contra de las disposiciones anti-perennización de la sección 3 de la Ley de Patentes de la India. Estima la tasa con la que la Oficina de Patentes de la India (OPI) erróneamente otorga tales patentes, y se documentan los argumentos para justificar la concesión de las patentes analizando el proceso por el que se procesan algunas patentes y el lenguaje que se utiliza en la solicitud de las patentes concedidas.
Las patentes secundarias que otorga la OPI
La mayoría (72%) de las patentes otorgadas para productos farmacéuticos son patentes secundarias, y se otorgan a productos que, comparados con otros medicamentos conocidos protegidos por patentes primarias, aportan beneficios marginales/
Cuadro 1. Patentes primarias versus secundarias: proporción y subcategorías
Patentes primarias + secundarias
Secundarias 72%, Primarias 28%.
Patentes secundarias
Formulación: 1206
Combinación: 297
Método de tratamiento: 63
Variante Física: 31
Utilización: 24
Isómero / enantiómero: 13
Sal: 11
Éster / éter / profármaco: 9
Se consideró que varios tipos de patentes secundarias violan distintas excepciones legales a la patentabilidad especificada en la sección 3, incluyendo las secciones 3 (d), 3 (e) y 3 (i).
| Excepciones a la patentabilidad | Frecuencia (% de las patentes) |
| 3 (d) Formulaciones, variante física, sales, ésteres / éter / profármaco, uso, isómero | 1294 (78%) |
| 3 (e) Combinaciones | 297 (18%) |
| 3 (i) Método de tratamiento. | 63 (4%) |
Las patentes secundarias que otorga la OPI
Solo se analizaron con detalle una pequeña fracción (15%) de las patentes secundarias otorgadas, y se acompañaron con una orden detallada, escrita, del Contralor. En la mayoría de los casos, la excepción a la patentabilidad relevante no se citó adecuadamente en la orden final escrita.
Solo una pequeña fracción (15%) de las patentes secundarias otorgadas fueron sometidas a un escrutinio detallado, acompañado por una orden detallada por escrito del Contralor. En la mayoría de los casos, la excepción relevante a la patentabilidad no se citó adecuadamente en la orden final escrita.
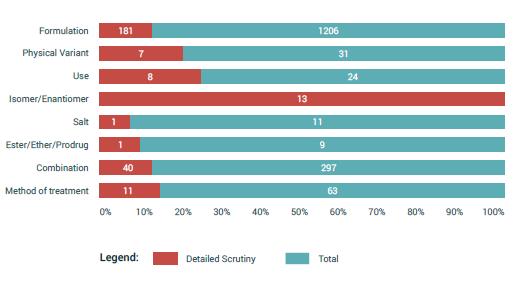
Figura 1. Ruta para producir nuestro informe
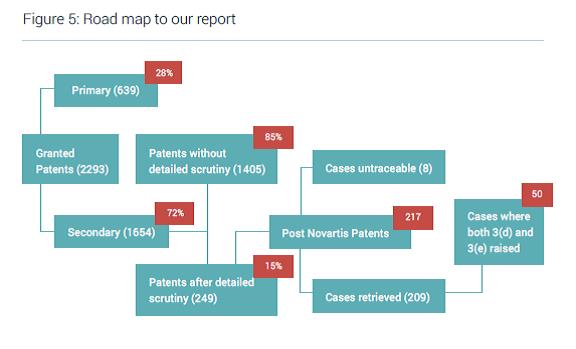
Los solicitantes ¿omiten los requisitos estrictos?
En 50 de los casos en que se realizó un escrutinio detallado, los solicitantes podrían haber demostrado una mejor eficacia terapéutica y sinergia para superar las secciones 3 (d) y 3 (e) respectivamente, que son las barreras establecidas a la patentabilidad.
Ningún solicitante entregó datos clínicos relevantes para demostrar la eficacia terapéutica, según lo estipulado por la decisión del Tribunal Supremo en relación con la patente secundaria de Novartis sobre el mesilato de imatinib en 2013.
Los solicitantes a menudo omitieron los estrictos requisitos de la sección 3 (d) ocultando las patentes secundarias como si fueran formulaciones y / o combinaciones. Esto ayudó a desviar el argumento de lo establecido en la sección 3 (d) hacia la sección 3 (e), ya que demostrar sinergia en la sección 3 (e) es relativamente más fácil en comparación con los requisitos de datos de eficacia de la sección 3 (d).
Tasa de error en la OPI
En la OPI hay inconsistencias en la forma como en la práctica se aplican los procesos, incluso cuando se trata de diferentes patentes secundarias para el mismo medicamento. Nuestro estudio anterior demostró varios casos en los que la OPI otorgó algunas patentes secundarias para un medicamento, mientras rechazaba otras. El uso de estándares diferentes puede afectar el acceso a medicamentos para una variedad de enfermedades.
Siete de cada 10 patentes otorgadas por la OPI se concedieron probablemente por error. Dado que ninguna de las solicitudes de patente secundaria presentó un documento adecuado y válido, todas ellas infringieron las disposiciones contra la extensión de las patentes de la ley de patentes de la India.
Conclusiones
En base a los resultados de este estudio, hemos concluido que la OPI tiene una tasa de error extremadamente alta en la concesión de patentes farmacéuticas, alrededor del 72%. Para concluir, se otorgaron 1654 patentes secundarias saltándose las disposiciones anti-extensión de las patentes y otros rechazos que podría haber planteado la OPI. Esto corresponde a una tasa de error tan alta como 72% de las patentes secundarias, de las cuales 1206 se otorgaron para formulaciones / composiciones, 297 para combinaciones, 88 para variantes físicas, usos, sales, isómeros, enantiómeros y profármacos, y 63% para un método de tratamiento.