El Acuerdo sobre los ADPIC —el tratado que establece las normas internacionales para la protección de la propiedad intelectual— cumplió 30 años este año. En sus tres décadas de aplicación, los estrictos requisitos de patentabilidad que impone el acuerdo a menudo han frustrado el acceso asequible a los medicamentos, en los países en desarrollo.
K.M. Gopakumar
La protección de los productos farmacéuticos mediante patentes se introdujo en los países en desarrollo para cumplir con el Acuerdo sobre los Aspectos de los Derechos de Propiedad Intelectual relacionados con el Comercio (ADPIC) de la Organización Mundial del Comercio (OMC). Como resultado, los productores farmacéuticos de los países en desarrollo perdieron la libertad de producir versiones genéricas de nuevos medicamentos. La eliminación de la libertad de operación ha comprometido considerablemente la capacidad de los países para poner a disposición de la población los últimos medicamentos eficaces a precios asequibles, lo que ha ampliado las disparidades en el acceso entre los países.
La pandemia de covid-19 puso de manifiesto estas contradicciones. No solo destacó la enorme desigualdad en el acceso a las vacunas, los tratamientos y las pruebas diagnósticas, sino que también evidenció la falacia de justificar el uso de las patentes como un mecanismo para recuperar la inversión en investigación y desarrollo (I+D). A pesar de contar con financiación pública de casi el 100%, los fabricantes de vacunas no estaban dispuestos a conceder licencias a gran escala para sus productos, lo que hubiera facilitado un acceso rápido. Por tanto, mientras que en octubre de 2021 los países de altos ingresos habían vacunado al 68% de sus habitantes, solo el 2,31% de la población de los países de bajos ingresos había recibido una dosis.
Este es solo uno de los muchos ejemplos de cómo se utiliza a las patentes para maximizar las ganancias, en detrimento de un acceso equitativo. El Comité de Políticas para el Desarrollo de las Naciones Unidas ha declarado que los derechos de propiedad intelectual “están sesgados a favor de recompensar a los innovadores, por encima de los consumidores”. La protección de la propiedad intelectual suele exceder con creces lo que sería necesario para incentivar la innovación, lo que da lugar a precios elevados, y a una oferta insuficiente de bienes públicos, además de reducir la difusión mundial de los beneficios de la innovación, lo que contribuye a generar nuevas desigualdades [1].
A nivel mundial, este régimen tiene un origen claro. Los 30 años de historia del Acuerdo sobre los ADPIC, que entró en vigor en 1995, son una historia de institucionalización del acceso desigual a los medicamentos, salvo algunas excepciones como los tratamientos contra el VIH/SIDA, la tuberculosis (TB) y la malaria. Pero incluso el acceso a los nuevos tratamientos contra el VIH/SIDA y la tuberculosis se ve amenazado por las patentes. Las iniciativas para facilitar el acceso, como el Fondo Global de Lucha contra el SIDA, la Tuberculosis y la Malaria (GFATM o Global Fund to Fight AIDS, TB and Malaria), y el Plan de Emergencia del Presidente de EE UU para el Alivio del SIDA (PEPFAR o US President’s Emergency Plan for AIDS Relief), se han visto interrumpidas porque la administración Trump ha retirado su financiamiento. Mientras tanto, la FDA ha aprobado un nuevo medicamento que puede prevenir eficazmente la infección por el VIH, lo que podría poner fin a las nuevas infecciones, pero las restricciones de las patentes podrían obstaculizar su potencial revolucionario. Del mismo modo, los medicamentos más eficaces que se han comercializado para el tratamiento del cáncer, las enfermedades raras y otras afecciones tienen un precio que está fuera del alcance de las personas de los países en desarrollo, en gran parte como resultado de la protección mediante patentes.
Por lo tanto, es urgente analizar las opciones que tienen los países en desarrollo, dada la creciente brecha en el acceso a los medicamentos.
Concentración en el mercado
La introducción universal de la protección por patentes de producto en 2005 —tal como lo exige el Acuerdo sobre los ADPIC, excepto en los países menos desarrollados— ayudó a las empresas farmacéuticas transnacionales a consolidar su poder en el mercado, al eliminar cualquier posibilidad de competencia procedente de las empresas de genéricos, en relación con los nuevos medicamentos. Al no haber competencia de genéricos, los titulares de las patentes podían cobrar precios muy elevados en los países desarrollados sin posibilidad de que se pudieran comparar los precios. La protección obligatoria de las patentes de producto también permitía a las empresas originarias obtener patentes en los países en desarrollo, sin ninguna obligación de comercializar el producto en ellos. Tras obtener las patentes, especialmente en aquellos países en desarrollo con capacidad de fabricación, como China y la India, las empresas originarias podían impedir que los fabricantes de genéricos produjeran nuevos medicamentos.
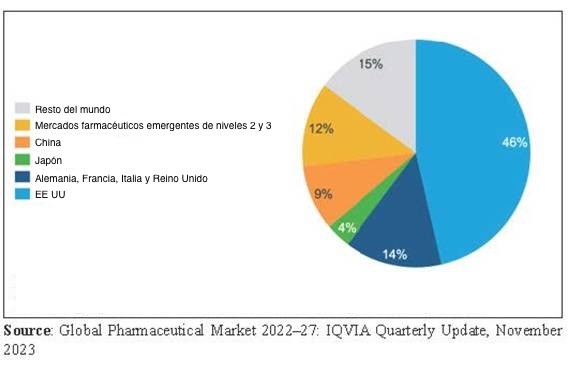
La figura 1 muestra la distribución del mercado farmacéutico (excluyendo las vacunas) entre las distintas regiones. El mercado está dominado por los países desarrollados: en términos de valor, EE UU, Europa y Japón representan alrededor del 64%. Esto pone de relieve que los titulares de patentes no han comercializado la mayoría de los nuevos medicamentos en los países en desarrollo. En el caso de los pocos productos que se comercializan, sus elevados precios los hacen inaccesibles para la población y los gobiernos de esos países en desarrollo. Así, los titulares de las patentes pueden obtener el máximo precio de los mercados de los países desarrollados — mediante la fijación de precios universales (un precio único aplicado globalmente)— e impedir que la población de los países en desarrollo tenga acceso a estos medicamentos patentados.
La concentración en el mercado de las vacunas es aún más acusada. Diez fabricantes representan el 73% del volumen de dosis de vacunas y el 85% del valor financiero mundial. Los fabricantes afiliados a la red de fabricantes de vacunas de los países en desarrollo representan el 50% de las dosis de vacunas adquiridas en todo el mundo, pero solo el 11% del valor financiero mundial. Por el contrario, los fabricantes afiliados a la Federación Internacional de Asociaciones y Fabricantes de Productos Farmacéuticos (IFPMA o International Federation of Pharmaceutical Manufacturers & Associations) representan el 34% del volumen, pero el 85% del valor financiero. Por países, los países de altos ingresos representan el 72% del valor financiero del mercado mundial de vacunas, que equivale a US$77.000 millones [2].
En 2024, el gasto mundial en medicamentos fue de US$1,7 billones, de los cuales US$1,4 billones correspondieron a los países desarrollados [3]. Los porcentajes correspondientes a los países con un gasto cada vez mayor en salud (los países “farmacéuticos emergentes o farmergentes”) [4] y a los países de bajos ingresos, fueron de US$312,200 millones y US$16,100 millones, respectivamente. De los US$1,421.500 millones que se gastaron en los países desarrollados, US$1,091.600 millones se destinaron a marcas originales. El gasto elevado en marcas originales se debe, en general, al gasto en medicamentos patentados, que no son asequibles para los gobiernos ni la población de los países en desarrollo.
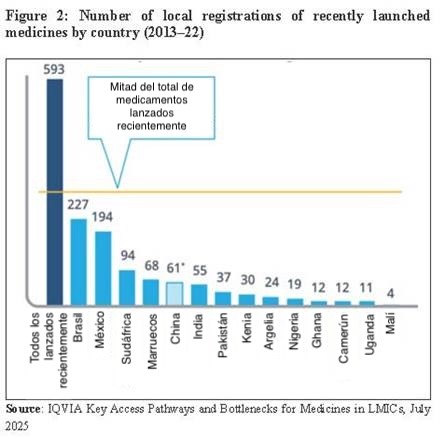
Los elevados precios, como resultado de la protección de las patentes de producto, han dado lugar a denegarel acceso a nuevos medicamentos en los países en desarrollo. Según un informe de la empresa de análisis sobre salud, IQVIA, de las 1.005 sustancias activas nuevas, introducidas en los últimos 20 años, el 81% se lanzaron en EE UU, seguido del 65% en Europa y el 60% en Japón [5]. Aunque China representó el 59%, casi el 40% se comercializó solo en ese país. El estudio ni siquiera menciona el porcentaje de nuevos lanzamientos en los países en desarrollo. Sin embargo, al citar otro informe de IQVIA, se afirma que solo en Brasil y México se comercializaron al menos el 30% de las sustancias activas nuevas más recientes (véase la figura 2). Esto demuestra claramente que las empresas originarias no están comercializando la mayoría de sus productos en muchos países en desarrollo (que son menos atractivos desde el punto de vista de las ganancias).
EE UU, Europa y Japón representan el 86,8% de las ventas de nuevos medicamentos que se han lanzado al mercado entre 2018 y 2023 [6]. El porcentaje del mercado farmacéutico emergente, que incluye a China y la India, es del 3,8%. El resto del mundo, incluyendo a Australia y Canadá, representa el 9,4%. Es evidente que se está negando el acceso a los nuevos medicamentos a las personas de los países en desarrollo. La mayoría de los pacientes y gobiernos de estos países no pueden comprar estos productos, independientemente de si hay una necesidad real.
La concentración del mercado farmacéutico también se refleja en las prioridades de I+D. Las empresas farmacéuticas se centran más en las necesidades en materia de salud de los mercados de los países desarrollados, que en las de los países en desarrollo. Por lo tanto, el régimen de patentes de producto no solo ha dado lugar a denegarel acceso, sino también a que no se hagan inversiones para desarrollar productos para enfermedades que afectan de manera desproporcionada a los países en desarrollo. Entre los que quedan excluidos por esta lógica de mercado se encuentran los 1,65 millones de personas que necesitan tratamiento para enfermedades tropicales desatendidas [7].
Por si fuera poco, a lo largo de los años, los fabricantes originarios han ideado diversas estrategias para extender su monopolio más allá de la fecha de vencimiento de las patentes originales:
A falta de medidas legalmente obligatorias para comercializar el producto a un precio asequible en los países en desarrollo, el Acuerdo sobre los ADPIC autoriza que se niegue el acceso a los nuevos medicamentos, con el fin de proteger la propiedad intelectual. Permite que las empresas creadoras saquen el máximo provecho de los mercados de los países desarrollados, sin tener que preocuparse por el precio comparativo de los genéricos. Esto aumenta la desigualdad en el acceso y compromete directamente la capacidad de los gobiernos, en particular de los países en desarrollo, para cumplir sus obligaciones internacionales en materia de derecho a la salud y derecho a la ciencia. En la práctica, esto se traduce en negarel acceso a los nuevos medicamentos para la gran mayoría de las personas que viven en los países en desarrollo, especialmente en los países de medianos y bajos ingresos, donde vive el 80% de la población mundial.
Respuesta legislativa y política
La respuesta legislativa y política habitual para abordar las preocupaciones derivadas de la protección de las patentes de producto, es el uso de las flexibilidades del los ADPIC. Las flexibilidades en las políticas que permite el Acuerdo sobre los ADPIC, disponibles durante las fases previa y posterior a la concesión de la protección mediante patente, se pueden utilizar para facilitar la disponibilidad de medicamentos genéricos a un precio asequible.
Las flexibilidades disponibles durante la etapa previa a la concesión ofrecen la posibilidad de establecer un umbral elevado para cumplir los criterios de patentabilidad. Esto se puede utilizar para frenar la práctica de solicitar múltiples patentes sobre la misma molécula y restringir el número de patentes (lo ideal sería una patente por molécula). Sin embargo, este enfoque solo ha tenido un éxito limitado en frenar la práctica de ampliar los monopolios.
Las flexibilidades disponibles durante la etapa posterior a la concesión incluyen las licencias obligatorias y de uso gubernamental, para facilitar la producción de versiones genéricas asequibles de los productos patentados. Un gobierno puede expedir dichas licencias para autorizar la producción o importación de genéricos sin el consentimiento del titular de la patente, con el fin de proteger la salud pública. Esta opción política puede invocarse, por ejemplo, durante situaciones de emergencia o cuando fracasan las negociaciones con el titular de la patente. El titular de la patente seguirá recibiendo regalías cuando se expida dicha licencia.
La importación paralela —otra flexibilidad del Acuerdo sobre los ADPIC— permite que un país importe un medicamento patentado de otro país donde se vende a un precio más bajo, sin necesidad del permiso del titular de la patente. Aunque la importación paralela se considera una flexibilidad importante, su eficacia real es dudosa debido a la política que siguen las empresas originarias de establecer precios universales.
El uso de las flexibilidades de los ADPIC para mitigar los efectos adversos de la protección por las patentes de producto obtuvo consenso político cuando los Estados miembros de la OMC adoptaron la Declaración de Doha relativa al Acuerdo sobre los ADPIC y la Salud Pública en 2001. La Declaración afirma que el Acuerdo sobre los ADPIC “puede y debe interpretarse y aplicarse de manera que respalde el derecho de los miembros de la OMC a proteger la salud pública y, en particular, a promover el acceso universal a los medicamentos. A este respecto, reafirmamos el derecho de los miembros de la OMC a utilizar plenamente las disposiciones del Acuerdo sobre los ADPIC, que ofrecen flexibilidades para tal fin”.
Sin embargo, en la práctica, los países enfrentan a muchos retos cuando quieren hacer uso de las flexibilidades de los ADPIC, especialmente en lo que respecta a las licencias obligatorias. A falta de capacidad de fabricación nacional, un país que expide una licencia obligatoria tiene que depender de un fabricante fuera de sus fronteras para el suministro del producto. Incluso si los productores del país son capaces de fabricar un determinado producto farmacéutico, es posible que tengan que obtener los ingredientes farmacéuticos activos (IFA o active pharmaceutical ingredients, API) de otro lugar. La protección mediante patente de los ingredientes farmacéuticos activos necesarios podría bloquear el suministro y, por lo tanto, hacer que la licencia obligatoria sea ineficaz.
El Acuerdo sobre los ADPIC se modificó en 2017 con el fin de que los países sin capacidad de fabricación nacional en el sector farmacéutico, puedan utilizar las licencias obligatorias de forma efectiva. Sin embargo, el sistema que se puso en marcha, en virtud de dicha modificación, está lleno de trámites complicados y es especialmente difícil de usar para los países con mercados pequeños, ya que no tienen economías de escala.
Como resultado de los diversos retos, la mayoría de los países en desarrollo no pueden utilizar eficazmente la opción de las licencias obligatorias. La situación se complica aún más cuando los titulares de patentes conceden licencias voluntarias a los fabricantes de genéricos en términos que les impiden suministrar a países de medianos ingresos, como Brasil o Malasia.
Además, las flexibilidades del Acuerdo sobre los ADPIC a menudo no se incorporan plenamente en las leyes nacionales o regionales sobre patentes. Por ejemplo, la figura 3 ilustra el estado de implementación de diversos criterios para la concesión de licencias obligatorias en 114 países. La tabla muestra que muchos países no establecen explícitamente los criterios para la concesión de una licencia de uso gubernamental. La falta de mención explícita de dichos criterios podría ocasionar que los titulares de patentes ejerzan una presión excesiva sobre esos países. Además, es posible que no existan medidas institucionales y políticas para aprovechar al máximo las flexibilidades. Por ejemplo, en la mayoría de los países en desarrollo no hay un mecanismo institucional eficaz para supervisar el impacto de las patentes de medicamentos en el acceso. Como resultado, los gobiernos de esos países no están en condiciones de adoptar medidas oportunas para facilitar el acceso a los nuevos medicamentos.
Otro ámbito en el que rara vez se utilizan las flexibilidades del Acuerdo sobre los ADPIC es el de los secretos comerciales. En virtud del artículo 39 del Acuerdo sobre los ADPIC, existe la obligación de mantener la confidencialidad de determinada información que aparece en los expedientes presentados para obtener la aprobación de la comercialización de medicamentos. Sin embargo, se estipula una excepción a esta norma general, en caso de que sea necesario proteger a los ciudadanos. Este artículo permite que las autoridades reguladoras compartan información confidencial para proteger la salud pública. Sin embargo, la mayoría de los países no incorporan excepciones a la cláusula de confidencialidad para los expedientes presentados para la aprobación de la comercialización.
El margen de maniobra en materia de políticas, con respecto al uso de las flexibilidades de los ADPIC, también se ve limitado por los tratados de libre comercio. Los tratados de libre comercio que incorporan disposiciones “ADPIC-plus” —obligaciones que van más allá de las establecidas en el Acuerdo sobre los ADPIC— eliminan o limitan el uso de las flexibilidades. Aunque algunos de los nuevos acuerdos incluyen texto en el que se establece que sus disposiciones en materia de propiedad intelectual no influyen en la libertad para hacer uso de las flexibilidades, los tratados de libre comercio suelen contener disposiciones sobre la concesión de patentes de nuevos usos, la extensión del plazo de las patentes y la vinculación de las patentes. Las patentes de nuevos usos permiten que las empresas amplíen sus derechos de monopolio patentando un nuevo uso de un medicamento existente, incluso cuando la patente original está a punto de expirar. Las extensiones del plazo de vigencia de las patentes prolongan los derechos exclusivos de una empresa, más allá del período estándar de 20 años, normalmente para compensar el tiempo que se tarda en obtener la autorización de comercialización. La vinculación de patentes liga el proceso de autorización de medicamentos al estado de las patentes, lo que impide que las autoridades de salud aprueben versiones genéricas hasta que todas las patentes del medicamento original hayan expirado, incluso si esas patentes son débiles o no están directamente relacionadas. Estas estipulaciones retrasan la entrada de medicamentos genéricos.
Una de las barreras más importantes que obstaculiza la aplicación de las flexibilidades de los ADPIC para facilitar el acceso a los medicamentos, es la presión política bilateral que se ejerce contra su uso. Los casos bien documentados de este tipo de presión llevaron al Panel de Alto Nivel sobre el Acceso a los Medicamentos del Secretario General de las Naciones Unidas a observar que “la presión política y económica que se ejerce sobre los gobiernos para que renuncien al uso de las flexibilidades del Acuerdo sobre los ADPIC viola la integridad y la legitimidad del sistema de derechos y obligaciones jurídicas creado por el Acuerdo, tal y como se reafirma en la Declaración de Doha. Esta presión socava los esfuerzos que hacen los Estados por cumplir sus obligaciones en materia de derechos humanos y salud pública” [8].
Un ejemplo claro es el informe anual Especial 301 sobre el estado mundial de la protección de la propiedad intelectual, publicado por la Oficina del Representante Comercial de EE UU (USTR o US Trade Representative), el organismo gubernamental estadounidense encargado de las cuestiones comerciales. Los países que hacen uso de las flexibilidades de los ADPIC pueden aparecer en la lista del informe y ser objeto de sanciones por parte de EE UU.
Más recientemente, el informe Especial 301 de 2025 que se publicó bajo la administración Trump desalentó el uso de licencias obligatorias, diciendo que “las acciones de los socios comerciales para emitir licencias obligatorias injustamente, amenazar con emitirlas, o animar a otros a emitirlas, generaban serias preocupaciones. Dichas acciones pueden socavar la propiedad intelectual del titular de la patente, reducir los incentivos para invertir en investigación y desarrollo de nuevos tratamientos y curas, y trasladar injustamente la carga de la financiación de dicha investigación y desarrollo a los pacientes estadounidenses y a los de otros mercados que respetan la propiedad intelectual como es debido… Dichas licencias no se deben utilizar como herramienta para aplicar políticas industriales —por ejemplo, ofreciendo ventajas a las empresas nacionales—, ni como influencia indebida en las negociaciones de precios entre los gobiernos y los titulares de derechos”.
Para evadir la presión política bilateral, los países en desarrollo como la India suelen evitar conceder licencias obligatorias y muestran su preferencia por las licencias voluntarias que emiten los titulares de las patentes. Sin embargo, una licencia voluntaria no solo suele excluir a los países de medianos ingresos, sino que también puede imponer condiciones restrictivas para impedir que el licenciatario suministre a territorios sin licencia, incluso en el marco de una licencia obligatoria. El Alto Comisionado de las Naciones Unidas para los Derechos Humanos ha señalado que este enfoque socava la igualdad de acceso a los medicamentos. Desde este punto de vista, las licencias voluntarias se utilizan como una herramienta para proteger las ganancias en lugar de promover el acceso.
Desafíos en materia de derechos humanos
Las presiones políticas bilaterales han disuadido a los países en desarrollo de expedir licencias obligatorias. A su vez, la incapacidad de los países en desarrollo para aprovechar al máximo las flexibilidades de los ADPIC compromete su capacidad para cumplir sus obligaciones en materia de derechos humanos, relacionadas con el derecho a la salud y el derecho a la ciencia. Además, el régimen de patentes del Acuerdo sobre los ADPIC conduce, en la práctica, a una discriminación en el disfrute de estos derechos por motivos de nacionalidad. Como se ha demostrado anteriormente, a la población de los países en desarrollo se le niega el acceso a los nuevos medicamentos debido a los elevados precios que se derivan de las patentes de producto.
El marco internacional de derechos humanos reconoce las implicaciones adversas del régimen mundial de propiedad intelectual, especialmente en lo que respecta al acceso a los beneficios de la investigación científica, entre los que se incluyen los medicamentos. El Comité de Derechos Económicos, Sociales y Culturales (CESCR o Committee on Economic, Social and Cultural Rights) de las Naciones Unidas, en su Observación general no. 25, adoptada en 2020, resalta que la propiedad intelectual no es innata, sino más bien un producto social que debe estar sujeto a los derechos a la salud, la alimentación y la educación.
Sin embargo, la mayoría de las leyes nacionales sobre patentes no establecen ningún proceso para que los pacientes o los grupos de pacientes inicien un procedimiento de licencia obligatoria. Por lo tanto, el disfrute del derecho a la salud y el derecho a la ciencia, en el contexto de los medicamentos patentados, depende de los modelos de negocio de las empresas farmacéuticas o de la discreción de los gobiernos nacionales.
Si se deja a la discreción de los gobiernos, el deber de proteger el derecho a la salud —recogido en el artículo 12 del Pacto Internacional de Derechos Económicos, Sociales y Culturales— se ve seriamente socavado. La Observación general no. 14 del Comité de Derechos Económicos, Sociales y Culturales establece que los países no solo deben promover activamente el derecho a la salud, sino que también actuar para garantizar que terceros no interfieran en el ejercicio de derecho a la salud, como las entidades privadas. En lo que respecta a los sistemas de salud privados, según el Comité de Derechos Económicos, Sociales y Culturales, se requiere la intervención del Estado para garantizar “la disponibilidad, accesibilidad, aceptabilidad y calidad de las instalaciones, los bienes y los servicios de salud”, y para “controlar la comercialización de equipos médicos y medicamentos por parte de terceros”.
Sin embargo, no existen medios directos disponibles en el marco de la propiedad intelectual (especialmente en las leyes nacionales y regionales sobre patentes), para que las personas afectadas puedan remediar la falta de acceso asequible a los medicamentos patentados. A nivel nacional, la administración de las patentes suele recaer en el Ministerio de Industria o Comercio, que puede considerar el uso de flexibilidades como una opción y no como una medida obligatoria que se utiliza para facilitar el acceso a los medicamentos. Teniendo en cuenta esta situación, el Relator Especial de las Naciones Unidas en el ámbito de los derechos culturales ha declarado: “Las exclusiones, excepciones y flexibilidades previstas en el derecho internacional sobre la propiedad intelectual —como el Acuerdo de la Organización Mundial del Comercio sobre los Aspectos de los Derechos de Propiedad Intelectual relacionados con el Comercio— siguen siendo opcionales desde la perspectiva del derecho mercantil, pero desde la perspectiva de los derechos humanos deberían considerarse obligaciones”. El enfoque opcional dentro del marco de la propiedad intelectual ha dado lugar a que las personas o los pacientes queden excluidos de la posibilidad de solicitar licencias obligatorias como remedio contra el abuso de los monopolios de patentes.
En este contexto, los activistas están presionando para que se respete el derecho a la salud. En la India, por ejemplo, hay al menos tres series de peticiones pendientes en dos cortes supremas, que buscan una solución a la violación del derecho fundamental a la salud mediante la emisión de licencias de uso gubernamental. Estas peticiones argumentan que el gobierno de la India no tiene discreción cuando se trata de facilitar el acceso a medicamentos patentados críticos, ya que la falta de acceso infringe los derechos fundamentales establecidos en el artículo 21 de la Constitución de la India. El artículo 21 garantiza el derecho a la vida, que ahora se extiende al derecho a vivir con dignidad, incluyendo el derecho a la salud. Por lo tanto, se argumenta que el Gobierno debería adoptar medidas en virtud de la Ley de Patentes del país para facilitar el acceso, como la concesión de una licencia de uso gubernamental. Los tribunales aún no han examinado a fondo las peticiones ni han dictado sentencia. En la figura 4 se detallan los medicamentos concretos que son objeto de estas peticiones.
Conclusión
En sus tres décadas de aplicación, el Acuerdo sobre los ADPIC ha consolidado importantes desigualdades en el acceso a los medicamentos, lo que ha perjudicado especialmente a los países en desarrollo. Si bien las flexibilidades de los ADPIC, como las licencias obligatorias, ofrecen vías legales para mitigar estos retos, los obstáculos para ejercerlas, , incluyendo las presiones políticas, la capacidad de fabricación limitada y los engorrosos marcos regulatorios, han limitado gravemente su eficacia.
Todos estos factores han tenido un efecto desalentador sobre el uso efectivo de las flexibilidades de los ADPIC. Sin embargo, la inestabilidad generada por las políticas de la administración Trump ha vuelto a centrar la atención en el uso de estas flexibilidades para facilitar el acceso asequible a los medicamentos. El uso de flexibilidades como las licencias obligatorias, para remediar el uso abusivo de las patentes, ofrece una herramienta eficaz para tomar represalias contra las medidas comerciales unilaterales desencadenadas en Washington.
Para abordar las desigualdades provocadas por las patentes de medicamentos se requiere un compromiso colectivo a nivel mundial para reformar el régimen de propiedad intelectual, haciendo mayor hincapié en las obligaciones en materia de salud pública y derechos humanos. Al mismo tiempo, deben renovarse los esfuerzos para generar la voluntad política necesaria para aprovechar las flexibilidades del Acuerdo sobre los ADPIC, con el fin de detener urgentemente la creciente desigualdad en el acceso a medicamentos y tratamientos eficaces. Con este fin, la comunidad internacional debe oponerse activamente a las presiones políticas y empresariales que socavan el derecho a la salud y el derecho a la ciencia. La mejor manera es empoderar a las personas, individual o colectivamente, con recursos legales contra los abusos derivados de las patentes, como los precios exorbitantes de los productos patentados, añadiendo disposiciones adecuadas a tal efecto en las leyes de patentes. Solo mediante esfuerzos tan exhaustivos se podrá cumplir la promesa de un acceso equitativo a los medicamentos y otros avances científicos.
K.M. Gopakumar es investigador sénior y asesor jurídico de Third World Network.
El autor agradece los comentarios y aportaciones de Chetali Rao, Rajnia de Vito y Srinath Namboodiri.
Notas