Los compuestos “me-too” o “próximos en su clase” son fármacos con mecanismos de acción similares. Si bien pueden aportar algunas ventajas, como una mayor eficacia o tolerancia, estas ventajas podrían ser teóricas, sin evidencia comparativa directa.
En este trabajo, publicado en la edición de septiembre de JAMA Internal Medicine [1], nuestra pregunta de investigación fue simple: ¿con qué frecuencia los ensayos clínicos aleatorizados (ECA) comparan “fármacos subsiguientes en la misma clase” con “fármacos primeros en su clase terapéutica”?
De 332 aprobaciones de la FDA entre 2009 y 2020, incluimos 94 aprobaciones de un compuesto “subsiguientes en su clase”. Descubrimos que 27 ensayos incluyeron un ensayo aleatorizado con un compuesto equivalente de su clase, pero solo 6 ensayos (6%) demostraron aportar una ventaja en la supervivencia.
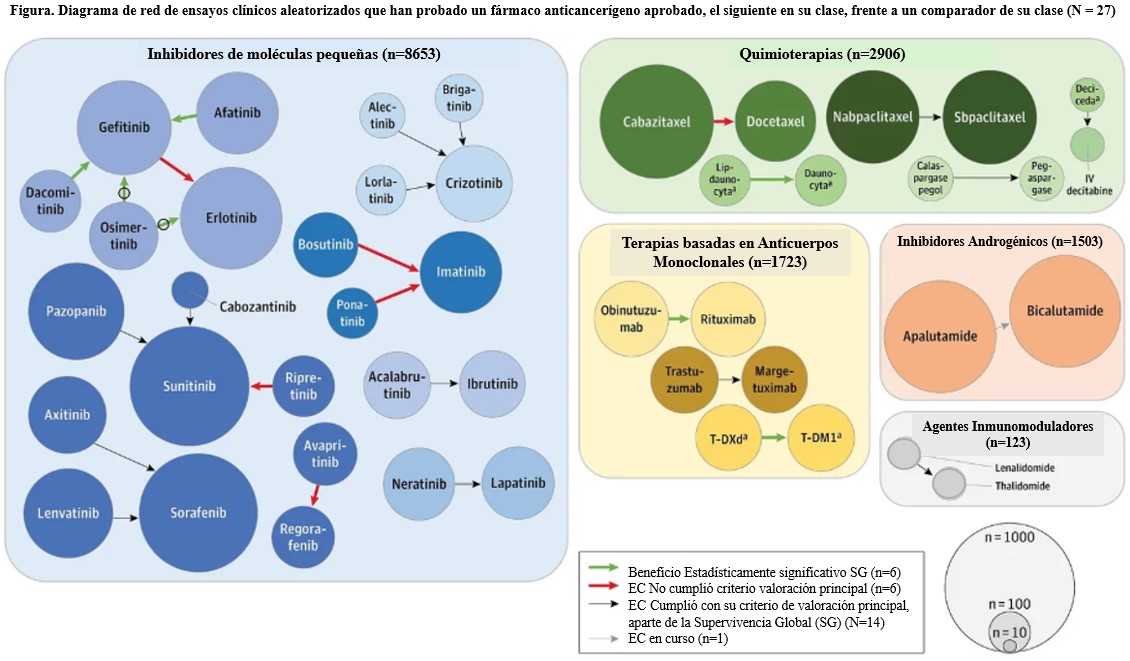
A continuación, se muestra la figura clave: el tamaño de los círculos representa el número de pacientes para un compuesto específico y las flechas representan los ensayos comparativos.
El color de las flechas indica si:
Verde: El ensayo mostró una ganancia de supervivencia (6 ensayos),
Rojo: No cumplió con su criterio de valoración principal (¡6 ensayos!) o
Negro: Cumplió con su criterio de valoración principal, aparte de la Supervivencia Global (14 ensayos).
Gris: ensayos en curso (1)
Sin embargo, en muchos casos, no se realizaron ECA comparativos, lo que dificulta la evaluación del verdadero valor terapéutico de los fármacos de nueva generación.
Nuestra conclusión:
«Estos resultados sugieren la necesidad de que los organismos reguladores incentiven los ECA dentro de la misma clase.
Esta evidencia ayudaría a determinar si los fármacos de nueva generación aportan avances significativos en la atención oncológica.
Esto es especialmente importante dado que los fármacos imitadores no han generado competencia de precios en oncología, y muchos se aprueban con los resultados de ensayos de un solo grupo o estudios con controles subóptimos. Aunque no siempre es posible si el desarrollo de fármacos se produce simultáneamente, los futuros marcos regulatorios deberían considerar la obligatoriedad de realizar ensayos comparativos entre los fármacos de la misma clase siempre que sea posible».
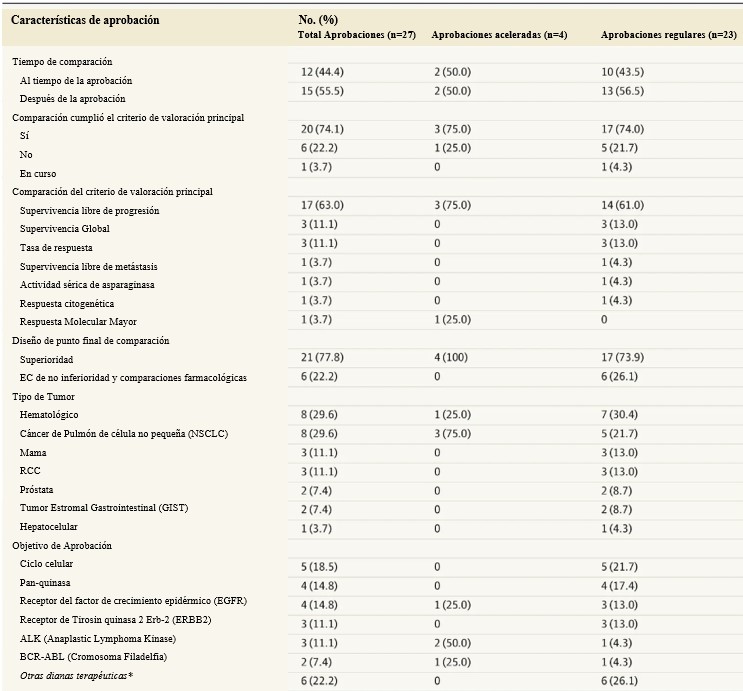
Consulte nuestro artículo completo publicado en JAMA Internal Medicine para obtener resultados más granulares, incluido un desglose por tipo de aprobación (acelerada/regular) como se ve en la tabla a continuación, enlace gratuito aquí: https://drive.google.com/file/d/139XBSqMB0CUguO-AV-zLR1zyTiFVotJE/view
Cuadro. Características de aprobación y de los estudios clínicos de fármacos antineoplásicos subsiguientes en su clase, aprobados por la FDA de EE UU, con ensayos que incluyeron comparadores dentro de la misma clase terapéutica
Referencias