Según un informe de Transperimed publicado hoy [1], más de la mitad de los resultados de los ensayos clínicos relacionados con Covid que se están implementando en Europa tienen un alto riesgo de acabar siendo investigación desperdiciada.
De un total de 118 ensayos clínicos con posibles tratamientos farmacológicos, 79 están en manos de empresas e instituciones que no tienen experiencia en publicar resultados en el registro europeo de ensayos clínicos.
Esto significa que es posible que los resultados de sus ensayos relacionados con Covid no se publiquen, especialmente si los medicamentos estudiados no muestran beneficios o los ensayos se concluyen antes de tiempo.
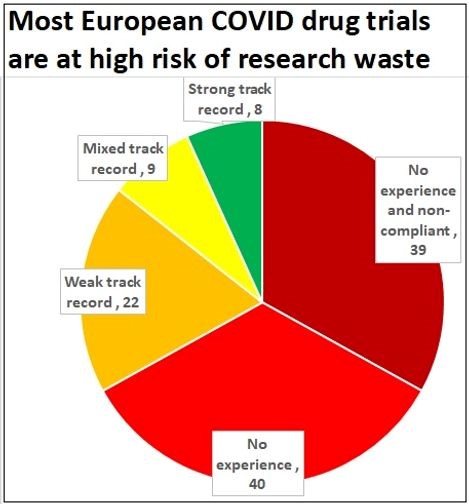
La mayoría de los ensayos de medicamentos para COVID en Europa tienen un alto riesgo de convertirse en investigación desperdiciada. Sin experiencia y sin adherirse a las normas de publicación, 39. Sin experiencia, 40. Historial corto, 22. Historial mixto, 9. Historial fuerte, 8.
Los ensayos que se terminan antes de tiempo, antes de que inscribir al número deseado de pacientes, son especialmente preocupantes.
Estos ensayos, por el pequeño tamaño de su muestra, a menudo son de poco interés para las revistas médicas más conocidas, por lo que los investigadores tienen pocos incentivos para publicar los resultados. Sin embargo, en conjunto, los resultados de muchos ensayos pequeños pueden aportar información valiosa y potencialmente vital sobre la efectividad y la seguridad de los posibles tratamientos contra Covid.
Como en la mayoría de los países europeos la primera ola de infecciones fue menos severa de lo esperado, se generó “escasez” de pacientes, por lo que es probable que muchos ensayos Covid se cierren antes de tiempo.
Según las normas de la Unión Europea, los resultados de estos ensayos deben publicarse en el registro europeo de ensayos EudraCT. En teoría, esto debería garantizar el acceso de la comunidad científica a los resultados de todos los ensayos Covid, incluso cuando no se publican en revistas médicas.
Sin embargo, como las agencias reguladoras de medicamentos de los diferentes países miembros de la UE no exigen que se cumplan estas normas, por lo general la adherencia es baja.
Al analizar de cerca los ensayos Covid que se están realizando en España y Francia se detectan muchos problemas.
Las agencias reguladoras nacionales de estos dos países son responsables de supervisar más de la mitad de los 118 ensayos clínicos de Covid que se hacen en Europa: 48 en España y 22 en Francia.
Ensayos clínicos con medicamentos para COVID en Europa, por país
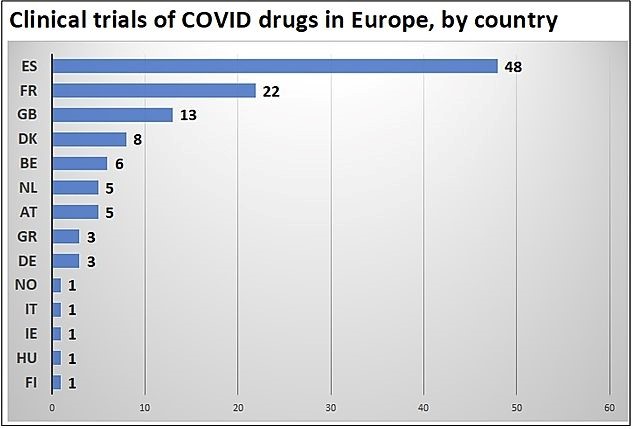
De los 48 ensayos con Covid en España, 46 están en manos de patrocinadores que nunca han publicado resultados en el registro.
Ningún patrocinador de los ensayos Covid que se están haciendo en España cumple totalmente con las normas de transparencia europeas, lo que indica que la agencia reguladora española, la AEMPS está haciendo poco o nada para obligar a que se cumplan las normas.
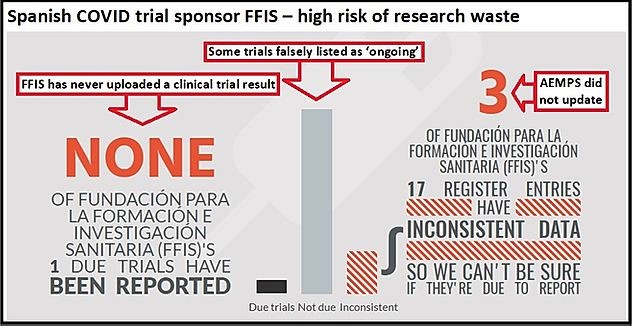
Por ejemplo, FFIS, un centro público de investigación está violando las reglas de transparencia, y no ha actualizado sus datos de registro. FFIS está ejecutando dos ensayos Covid.
El panorama es similar en Francia, donde la agencia reguladora nacional ANSM es responsable de supervisar 22 ensayos Covid.
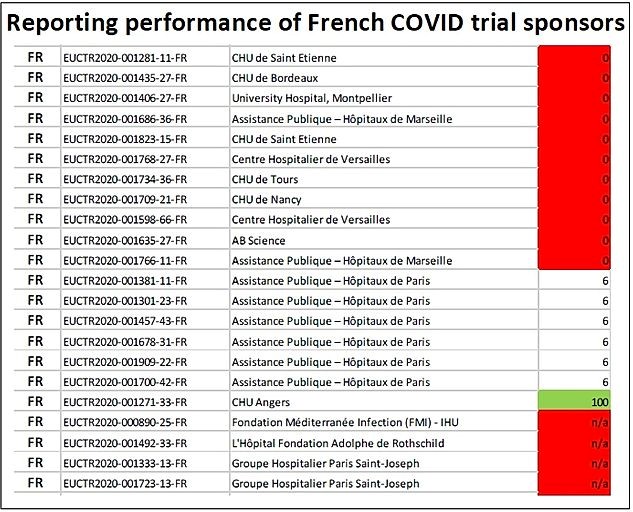
Solo uno de los patrocinadores de esos ensayos, CHU d’Angers, parece cumplir totalmente con las normas de transparencia. Seis ensayos están patrocinados por Assistance Publique – Hôpitaux de Paris, que no ha publicado los resultados de más del 90% de los ensayos que ha realizado. Ninguno de los otros patrocinadores franceses ha publicado los resultados de los ensayos.
Informe del desempeño de los patrocinadores franceses de ensayos de COVID.
En respuesta al informe, Thomas Senderovitz, director general de la Agencia Danesa de Medicamentos y presidente del grupo de Jefes de las Agencias [Europeas] de Medicamentos (hma.eu), dijo a STAT News [2] que:
“[Es] justo alertar y recordar a todos que tienen que publicar los resultados de los ensayos clínicos, tal como lo indica la legislación. Nos tomamos muy en serio que los patrocinadores sean muy meticulosos al presentar sus resultados”.
Till Bruckner, fundador de TranspariMED, dijo:
“Ocultar los resultados de los ensayos clínicos amenaza con socavar la búsqueda de tratamientos seguros y eficaces contra Covid-19. Actualmente, en toda Europa, se están gastando miles de millones de euros provenientes de fondos públicos en investigación médica, pero esas inversiones solo beneficiarán a los pacientes si se publican los resultados”.
“Claramente, muchas agencias reguladoras nacionales han descuidado su responsabilidad de garantizar que las empresas y centros de investigación publiquen todos los resultados de los ensayos clínicos”.
“Es urgente que los reguladores nacionales intensifiquen y comiencen a monitorear de cerca los ensayos Covid-19 que están bajo su supervisión, e impongan sanciones a aquellos patrocinadores de ensayos que violen las normas”.
Jaume Vidal, Asesor Principal de Políticas para los Proyectos Europeos de Acción Internacional para la Salud (Health Action International), dijo:
“La falta de transparencia en informar los resultados de los ensayos clínicos sigue siendo un obstáculo para el progreso científico. No hay necesidad de poner obstáculos adicionales cuando se está enfrentando una pandemia de proporciones globales. Las autoridades tienen el deber y la obligación moral de hacer cumplir las normas vigentes relacionadas con la divulgación adecuada de tan importante información, incluyendo los patrocinadores, protocolos y resultados (entre los que figuran los informes de los ensayos clínicos – clinical study reports) de todos los ensayos clínicos realizados en sus jurisdicciones”.
Las instituciones europeas que hacen ensayos para el Covid pueden encontrar una guía práctica para gestionar el registro de los datos de los ensayos y cargar sus resultados en EudraCT en el sitio web de TranspariMED [3].
Puede acceder al informe completo de TranspariMED, incluida la lista completa de los 118 ensayos clínicos de Covid registrados en Europa en el enlace que aparece en la referencia [1]
Referencias