Las crisis mundiales y regionales exigen soluciones rápidas y flexibles, especialmente cuando se trata del acceso a medicamentos vitales para responder a una emergencia de salud. El 30 de diciembre de 2025, el Parlamento Europeo publicó la revisión de un reglamento sobre licencias obligatorias para gestionar las crisis [1]. Una licencia obligatoria es una autorización que otorga el gobierno para utilizar o producir un producto patentado, sin el consentimiento del titular de la patente. El objetivo de este nuevo reglamento europeo es abordar de manera eficiente las crisis de salud en la Unión Europea (UE), mejorando el acceso en toda la región a “productos relevantes para responder a las crisis” [2].
Antes de esta nueva regulación para el ámbito regional, las licencias obligatorias solo se podían conceder a nivel de país y estaban pensadas para satisfacer las necesidades de una nación concreta. La pandemia de covid-19 puso de manifiesto la importancia de contar con mecanismos de coordinación regional para afrontar una emergencia de salud de mayor alcance. Sin embargo, más allá del contexto específico de las crisis de salud, la colaboración y la coordinación regional en materia de licencias obligatorias es esencial para garantizar la suficiencia del suministro y la asequibilidad de los productos para la salud.
Las licencias obligatorias han sido un instrumento del derecho de la propiedad intelectual desde hace tiempo, que se pueden utilizar cuando los países consideran que los titulares de patentes no están “explotando” suficientemente su invención o están abusando de sus derechos de patente [3]. Aunque el Acuerdo sobre los Aspectos de los Derechos de Propiedad Intelectual relacionados con el Comercio (Acuerdo sobre los ADPIC) de la Organización Mundial del Comercio (OMC) impone nuevos requisitos a los Estados miembro para la concesión de patentes y otros tipos de protección de la propiedad intelectual para las invenciones farmacéuticas. También incluye una disposición (Artículo 31) que permite que los Estados miembro adopten leyes sobre licencias obligatorias en sus propias leyes nacionales de propiedad intelectual [4].
El derecho a conceder licencias obligatorias es una de las “flexibilidades” más debatidas del Acuerdo sobre los ADPIC. Los Estados miembro pueden conceder licencias obligatorias en casos tales como la falta de uso de una patente, la conducta anticompetitiva del titular de la patente, para responder a necesidades de interés público en situaciones de emergencia, o para uso gubernamental no comercial (a menudo denominadas licencias de “uso gubernamental”). Aunque estas normas distan mucho de ser perfectas, cabe señalar que la mayoría de los países del mundo han adoptado alguna versión de estas leyes [5].
En un informe reciente, investigadores del Grupo de Trabajo sobre Tratados de Comercio e Inversión y Acceso a los Medicamentos (Trade and Investment Treaties and Access to Medicines), del Centro de Políticas de Desarrollo Global de la Universidad de Boston (Boston University Global Development Policy Center), analizan en qué medida un conjunto seleccionado de países de medianos ingresos ha incorporado disposiciones clave del Acuerdo sobre los ADPIC en sus propias leyes de licencias obligatorias [6, 7].
Esta investigación compara la redacción de las leyes de diferentes países y luego las evalúa en función de una lista más completa de disposiciones sobre licencias obligatorias que podrían contribuir a facilitar el acceso a los productos para la salud, y que se consideran mejores prácticas. Aunque todos los países estudiados habían adoptado alguna ley relacionada, hay grandes diferencias en la adopción de diversos aspectos positivos de dichas leyes, y los países se podrían beneficiar incorporando más flexibilidades relevantes para la salud.
Antecedentes del uso de las licencias obligatorias
A pesar de las flexibilidades explícitas que se incorporaron en el Acuerdo sobre los ADPIC para la concesión de licencias obligatorias, durante mucho tiempo, cuando los países de medianos y bajos ingresos han intentado utilizar estas herramientas, se han tenido que enfrentar a la oposición de las empresas farmacéuticas y de los países de altos ingresos [8, 9].
Tras la indignación pública que se produjo a finales de la década de 1990 y principios de la del 2000, los miembros de la OMC se unieron para reafirmar su derecho a conceder licencias obligatorias, en virtud del acuerdo [10]. Por ejemplo, la Declaración de Doha relativa al Acuerdo sobre los ADPIC y la Salud Pública, adoptada en 2001, dejó claro que los países tenían derecho a elegir sus propios motivos para expedir licencias obligatorias y que podían dar prioridad a la salud pública y al acceso universal a los medicamentos [11].
En los años siguientes, los mecanismos de licencia obligatoria se emplearon con mayor frecuencia. Ese esfuerzo pareció decaer tras la creación del Banco de Patentes de Medicamentos (Medicines Patent Pool o MPP) en 2010 [12]. A través del Banco de Patentes de Medicamentos se conceden licencias voluntarias a un grupo reducido de empresas para que fabriquen y exporten a una lista fija de países autorizados por la empresa farmacéutica original. Esta lista a menudo excluye a muchos países de ingresos medianos altos comercialmente atractivos, ya que las empresas originales suelen tratar de limitar la competencia de los medicamentos genéricos en esos mercados, para poder seguir siendo las únicas que pueden obtener beneficios comerciales.
Incluso durante la pandemia de covid-19, los países se apoyaron principalmente en la concesión de licencias voluntarias para ampliar la fabricación de pruebas diagnósticas, vacunas y, finalmente, tratamientos. Paradójicamente, los países más ricos figuraron entre los pocos que se apresuraron en recurrir a su legislación para anular los derechos de patente, con el fin de hacer frente a las necesidades derivadas de la pandemia [13]. Mientras tanto, un número cada vez mayor de países, encabezados por Sudáfrica y la India, presionaron para que se suspendieran las restricciones del Acuerdo sobre los ADPIC, con el fin de facilitar la anulación de los derechos de patente de manera más general [14].
Justificación del estudio
Dado que los países de medianos ingresos suelen estar excluidos de las licencias voluntarias, y experimentan obstáculos adicionales para acceder a los medicamentos, los miembros del Grupo de Trabajo habían recomendado anteriormente que se hiciera más investigación para comprender por qué se infrautilizan las licencias obligatorias [15]. La investigación publicada en nuestro informe pretendía explorar si las leyes vigentes en estos países podían dificultar la concesión de licencias obligatorias más de lo necesario, o si eran lo más amplias posible dentro de las restricciones del Acuerdo sobre los ADPIC.
El estudio examinó en qué medida los países que suelen quedar excluidos de las licencias voluntarias han incorporado las flexibilidades del Acuerdo sobre los ADPIC en sus leyes nacionales de licencias obligatorias, de manera que dichas leyes sean tan eficaces y fáciles de aplicar como lo permiten las normas internacionales [16]. Entre los países evaluados se incluyen Argelia, Argentina, China, Colombia, Ecuador, Jordania, Malasia, México, Panamá, Perú, Filipinas, Rumanía, Tailandia, Turquía y Ucrania, que en el pasado han quedado excluidos de las licencias voluntarias del Banco de Patentes de Medicamentos
Diversidad en la incorporación de las flexibilidades del Acuerdo sobre los ADPIC
Con el fin de comparar las leyes de los distintos países, el informe divide las “mejores prácticas” en materia de legislación sobre licencias obligatorias en tres categorías: (1) la amplitud de los motivos aceptados para la concesión de licencias, (2) las flexibilidades procedimentales (que miden la facilidad general para aplicar la ley de licencias obligatorias) y (3) el alcance de la utilización (que mide la capacidad de utilizar la licencia de manera efectiva para mejorar el acceso a los medicamentos, tanto en el país que concede la licencia como fuera de él). Aunque los 15 países cuentan con leyes de licencias obligatorias, estas varían considerablemente en cuanto a la forma en que aplican dichas normas.
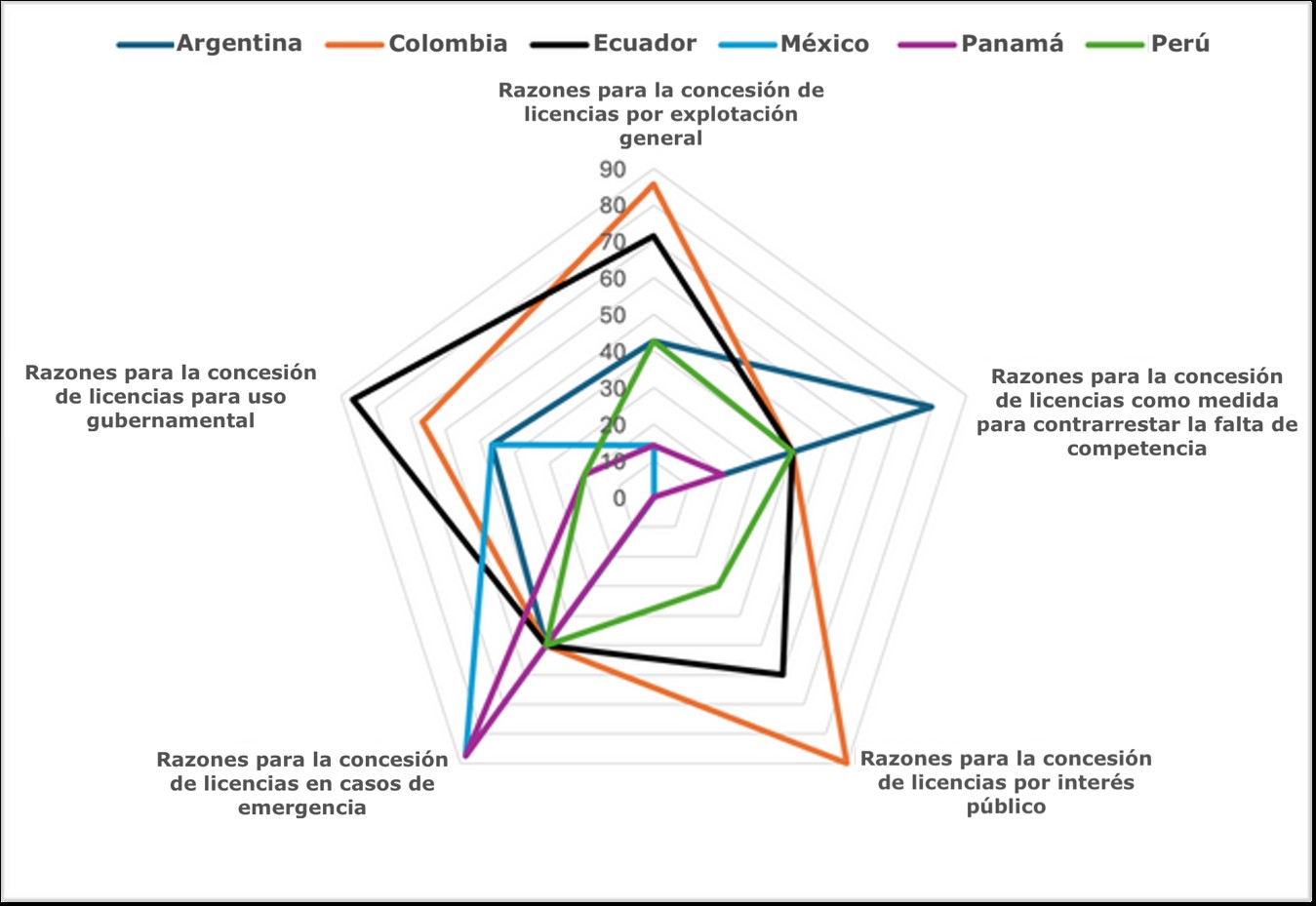
La Figura 1 ofrece un ejemplo visual de esta diversidad y pone de relieve la amplia variedad de motivos para conceder licencias obligatorias en los distintos países. La Figura muestra que México (azul claro) incluye muchos motivos diferentes para expedir licencias en situaciones de emergencia (el 87,5% del máximo, que se identifica como el mayor número de motivos de cualquier país incluido en el estudio), pero es tajante en no permitir que se concedan estas licencias como medida correctiva frente a la falta de competencia, ni por motivos de interés público. Colombia (naranja), por el contrario, incluye una amplia gama de motivos dentro de su licencia de interés público (el 90% del máximo), pero menos motivos para situaciones de emergencia que México. En esta figura, cuanto mayor es el área dentro de una forma determinada, más posibilidades tienen los países de conceder licencias obligatorias y, por lo tanto, mayor es el margen de maniobra política.
El informe reveló niveles similares de diversidad entre los países estudiados, tanto en la flexibilidad de los procedimientos como en el alcance de su uso. Los países que incorporan mucha flexibilidad en sus leyes para determinada categoría de prácticas, pueden tener muy poca flexibilidad en otra categoría. La ley de Perú (en verde), por ejemplo, establece motivos bastante limitados para la concesión de una licencia, y fue el único país de nuestro estudio que no hacía referencia a las emergencias de salud ni al acceso a los medicamentos como motivos para la concesión de licencias (véase la Tabla 5 del informe) [18]. Sin embargo, desde el punto de vista procedimental, la ley de Perú es una de las más sencillas de utilizar para solicitar y conceder este tipo de licencia (véase la Figura 2 del informe) [19].
La legislación nacional es solo el principio
Independientemente de la flexibilidad y la facilidad de aplicación de las leyes de licencia obligatoria de un país, existen muchos factores contextuales, más allá de la propia ley, que influyen en si realmente se utilizan para conceder licencias. Para analizar los factores extralegales que influyen, el informe incluye dos estudios de caso: Tailandia y Colombia. Estos estudios de caso ponen de manifiesto que, aunque ampliar el margen de maniobra en las leyes nacionales puede mejorar el acceso a los medicamentos, la concesión satisfactoria de licencias no depende únicamente de la calidad de la legislación.
Debido a la complejidad del panorama de las patentes y los secretos comerciales, las licencias obligatorias se pueden ver limitadas por la necesidad de acceder a múltiples patentes relacionadas y a conocimientos técnicos no divulgados que solo posee el titular original de la patente [20]. Es posible que los países carezcan de voluntad política a nivel interno, o que se vean sometidos a presiones políticas externas, de modo que la concesión de una licencia obligatoria no resulte políticamente viable [21, 22].
Del mismo modo, si la necesidad epidemiológica no es lo suficientemente acuciante en un país concreto, es posible que no exista un apoyo generalizado para la concesión de una licencia [23]. En ocasiones, los requisitos regulatorios plantean obstáculos adicionales, debido a que no se han armonizado a nivel transfronterizo [24, 25].
Por último, incluso si se han superado todos esos obstáculos, es posible que un país no disponga por sí solo de capacidad técnica y financiera suficiente para superar las barreras comerciales [26]. Este último obstáculo puede ser especialmente importante, ya que la mayoría de los países de medianos y bajos ingresos tienen mercados nacionales reducidos [27]. A menudo estos carecen de una población lo suficientemente numerosa como para que por sí solos resulten económicamente atractivos para uno o más fabricantes de genéricos.
Las licencias obligatorias regionales de la UE: un ejemplo a seguir
Los países que se enfrentan a cada uno de estos obstáculos deberán implementar diversas soluciones políticas. Una recomendación política especialmente destacada que se hace en el informe es que los países de medianos ingresos cooperen para incorporar buenas prácticas en sus legislaciones y colaboren en la concesión de licencias, con el fin de crear mercados agregados y generar economías de escala para los fabricantes de medicamentos genéricos.
Aunque la mayoría de los grandes países europeos no se enfrentan a los mismos obstáculos mencionados anteriormente, el Parlamento de la UE ha reconocido el valor de cooperar a nivel regional para responder a una crisis de salud, agregando demanda y acelerando el acceso. Los países de medianos y bajos ingresos podrían adoptar un mecanismo de este tipo en sus propios acuerdos de integración regionales y megarregionales.
Tanto en el Tratado Continental Africano de Libre Comercio (African Continental Free Trade Agreement) como en la Asociación de Naciones de Asia Sudoriental (Association of Southeast Asian Nations) se están llevando a cabo negociaciones que podrían abordar la necesidad de que cada región desarrolle una política de propiedad intelectual y un mecanismo de licencias obligatorias a escala regional [28, 29]. Al seguir los pasos de la UE, podrían mejorar notablemente los resultados en materia de salud, para sus Estados miembro, y estar mejor preparados para la próxima crisis mundial de salud.
Referencias