Profeco y Cofepris alertan por comercialización ilegal de productos con tirzepatida
Procuraduría General del Consumidor, 11 de marzo de 2026
https://www.gob.mx/profeco/prensa/profeco-y-cofepris-alertan-por-comercializacion-ilegal-de-productos-con-tirzepatida
Tags: falsificación de tirzepatida, comercialización ilegal de tirzepatida, Rapha, Dr. Pen y Peptide Xperts
Se comercializan a través de plataformas de comercio electrónico, sitios web y aplicaciones de dispositivos móviles, sin que cuenten con registro sanitario para su distribución en territorio nacional.
La Procuraduría Federal del Consumidor (Profeco) comparte la alerta que emitió la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) sobre la comercialización ilegal de tres productos con Tirzepatida a través de plataformas de comercio electrónico, sitios web y aplicaciones de dispositivos móviles.
La Cofepris emitió esta alerta sanitaria luego de recibir el análisis técnico-documental de la información presentada por el importador Eli Lilly y Compañía de México, S.A. de C.V., que identificó la venta ilegal.
Se trata de los productos marca Rapha, Dr. Pen y Peptide Xperts que se ofertan en distintas presentaciones, como gotas, parches, viales, jeringas prellenadas, sin que cuenten con registro sanitario para su distribución en territorio nacional.
La Cofepris subraya que la adquisición y uso de tirzepatida debe realizarse bajo prescripción, de conformidad con el artículo 226 de la Ley General de Salud que clasifica los medicamentos para su venta y suministro y advierte que su uso indiscriminado y sin supervisión de un médico especialista, puede ocasionar un estrés o sobreactividad en órganos como el hígado o el páncreas, entre otros, lo que puede generar un fallo en los mismos.
Ante el riesgo, la institución recomienda nunca adquirir estos productos en cualquier presentación y en caso de contar con información sobre su posible comercialización, realizar la denuncia sanitaria correspondiente.
En caso de estar utilizando los productos mencionados, se recomienda suspender de inmediato su uso y consultar con un profesional de la salud para una valoración médica.
Si alguna persona ya lo ha consumido y presenta reacciones adversas, se recomienda que lo reporte en el siguiente enlace: https://vigiflow-eforms.who-umc.org/mx/vigiramo al correo electrónico:farmacovigilancia@cofepris.gob.mx.
La alerta puede consultarse en: https://www.gob.mx/cms/uploads/attachment/file/1055652/Alerta_Sanitaria_Tirzepatida_09022026.pdf.
Alerta Sanitaria COFEPRIS. Comercialización ilegal del producto trikafta.
(elexacaftor, tezacaftor e ivacaftor), 100 mg, 50 mg y 75 mg; (ivacaftor) 150 mg comprimidos.
Comisión Federal para la Protección contra Riesgos Sanitarios, 3 de marzo de 2026
https://www.gob.mx/cms/uploads/attachment/file/1060524/Alerta_Sanitaria_trikafta_03032026.pdf
Tags: Trikafta, elexacaftor, tezacaftor, ivacaftor, comercialización ilegal de trikafta
Categoría: Alerta sanitaria de medicamentos
Lugar de expedición: Ciudad de México
La Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS) informa sobre la comercialización ilegal del producto trikafta® (elexacaftor, tezacaftor e ivacaftor) 100 mg, 50 y 75 mg; (ivacaftor) 150 mg, comprimidos.
Esta alerta sanitaria se emite derivada del análisis técnico-documental con base en la información proporcionada por el representante legal en México, que identificó la comercialización ilegal del producto trikafta® con número de lote W077103 y fecha de caducidad 04-2026, destinado originalmente a Uruguay.
Sin embargo, al comercializarse en territorio nacional, se desconoce si el producto fue importado ilegalmente o podría tratarse de una falsificación, debido a su bajo costo. Cabe destacar que, al ser un producto destinado a otro país, no cumple con el etiquetado autorizado para su venta en México, por lo que se desconocen las condiciones en las que fue importado, manipulado, almacenado y distribuido, lo que representa un riesgo para la salud de la población, ya que no se garantiza su calidad, seguridad y eficacia.
Por lo anterior, COFEPRIS emite las siguientes recomendaciones:
Población en general y profesionales de la salud:
Distribuidores y farmacias:
COFEPRIS mantendrá acciones de control sanitario e informará oportunamente a la población en caso de identificar nuevas evidencias, con el fin de prevenir riesgos a la salud de la población, procedentes de productos, servicios o establecimientos que incumplan con la legislación sanitaria vigente.
“El presente, se emite con fundamento en los artículos 4°, párrafo cuarto, de la Constitución Política de los Estados Unidos Mexicanos; 17 y 39, fracción XXI, de la Ley Orgánica de la Administración Pública Federal; 1, 17 Bis, fracción I, de la Ley General de Salud; y 3, 12 del Reglamento de la Comisión Federal para la Protección contra Riesgos Sanitarios.”
“De conformidad con el derecho a la protección a la salud y por principio precautorio, la Comisión Federal para la Protección contra Riesgos Sanitarios con la finalidad de reducir los riesgos sanitarios a la población, informa sobre situaciones que presentan un riesgo sanitario para la salud de la población en general, derivado del uso y/o consumo de diversos insumos para la salud, productos o servicios que no cumplen con la regulación sanitaria vigente.”
Arixtra: La AEMPS informa sobre un defecto de calidad y las precauciones a adoptar
Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), 6 de febrero de 2026
https://www.aemps.gob.es/informa/la-aemps-informa-sobre-un-defecto-de-calidad-en-el-medicamento-arixtra-y-las-precauciones-a-adoptar/
Tags: Viatris Pharmaceuticals, Arixtra, defecto de calidad Arixtra, eventos tromboembólicos venosos
Categoría: Medicamentos de uso humano, defectos de calidad
Referencia: ICM (CONT), 04/2026
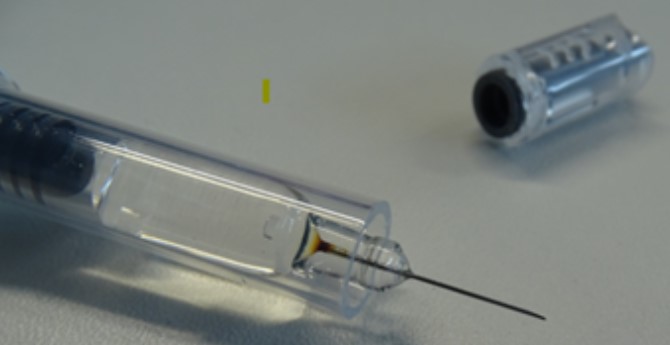
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha tenido conocimiento, a través del titular de autorización de comercialización del medicamento Arixtra, de un defecto de calidad en la aguja de las jeringas precargadas de este medicamento (ver foto).
El defecto ha sido detectado tras recibir notificaciones relacionadas con una coloración marrón y obstrucción en la aguja de las jeringas precargadas de este medicamento indicado para prevenir que se formen coágulos de sangre en los vasos sanguíneos. La causa de este defecto está relacionada con la presencia de una partícula de hierro que se ha oxidado en el interior de la aguja.
Actualmente, la investigación está en curso para identificar la causa raíz e implementar las acciones correctivas y preventivas correspondientes.
Se estima que el defecto es muy poco frecuente, no habiéndose recibido ninguna reclamación relacionada con este evento en España, y podría aparecer en cualquier lote de las presentaciones de Arixtra comercializadas en nuestro mercado:
Los riesgos potenciales del uso de una jeringa precargada con presencia de óxido incluyen falta de eficacia por obstrucción de la aguja, reacciones adversas si se administra la inyección afectada (reacciones de hipersensibilidad, complicaciones en el lugar de inyección, incluida rotura de aguja, efectos tromboembólicos e infecciones sistémicas).
Dependiendo de la dosis, Arixtra está indicado para:
Información para profesionales sanitarios
Información para farmacias
Datos de la empresa
Viatris Pharmaceuticals, S.L.
(+34) 900 102 712
Correo electrónico para notificar defectos de calidad: cliente@viatris.com, ReclamacionesQA.Spain@viatris.com
Correo electrónico para notificar sospechas de reacciones adversas: phvg.spain@viatris.com