Ensayos Clínicos
Investigaciones
La no-adherencia: influencia directa en la duración y costo del ensayo clínico
(Non-adherence: A direct influence on clinical trial duration and cost)
M. Alsumidaie
Applied Clinical Trials, 24 de abril de 2017
http://www.appliedclinicaltrialsonline.com/non-adherence-direct-influence-clinical-trial-duration-and-cost
Traducido por Salud y Fármacos
Entre las empresas biofarmacéuticas, las organizaciones que se dedican al desarrollo siempre se han preocupado por la larga duración y los costos de los ensayos clínicos, que siguen siendo caros y su duración continúa alargándose [1]. Aunque las iniciativas nuevas que tienen como objetico mejorar la eficiencia de los estudios y la calidad de los datos (por ejemplo, RBM, diseño de ensayos adaptativos y nuevos pilotos) prometen reducir la duración del ensayo y su impacto en los costos, la industria biofarmacéutica está pasando por alto un elemento crítico que afecta los plazos del estudio: la no adherencia del paciente. En este artículo, comentamos sobre los costos de los ensayos clínicos, explicamos el impacto de la no adherencia en la duración del estudio, y propondremos un modelo para calcular el costo de la no adherencia.
Costos de los ensayos clínicos
Hay varias actividades que contribuyen a los presupuestos de los ensayos clínicos; desde la perspectiva general, estos costos incluyen costos por paciente (por ejemplo, gastos de reclutamiento y retención de pacientes), los costos vinculados al centro de investigación (como los honorarios de los investigadores, el personal del centro / los gastos administrativos, los honorarios del comité de ética, los honorarios del procedimiento) y los honorarios ligados al estudio (por ejemplo, los honorarios para la recolección de datos, el monitoreo, los salarios del personal del organismo patrocinador involucrado en el estudio y/o de la CRO, honorarios por enmiendas de protocolo y costos de proveedores) [2]. Sin embargo, aparte de que los atrasos en el cronograma del estudio aumentan inesperadamente los presupuestos del estudio, también disminuyen los ingresos por las ventas del nuevo producto, que en el caso de productos estratégicos (o nicho) pueden representar US$600.000 al día, y hasta US$8 millones diarios si se trata de productos médicos de gran éxito [3].
Figura 1. No adherencia al producto experimental en los ensayos clínicos [7]
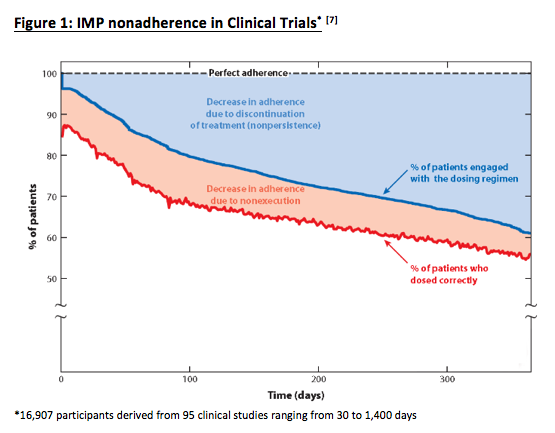
*16.907 pacientes participando en 95 ensayos con una duración entre 30 y 1.400 días
Figura 2. Impacto de la no adherencia [7]
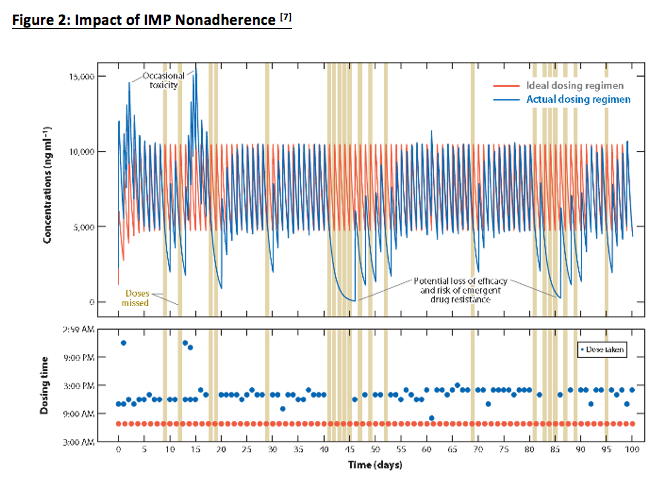
Prevalencia de no adherencia al estudio
Sería ideal si todos los pacientes siguieran las indicaciones de cómo deben consumir los productos médicos en investigación (PIM) y el protocolo del estudio, sin embargo, muchos pacientes no lo hacen. La Figura 1 ilustra que aproximadamente 40% de los pacientes dejan de consumir los productos en investigación de la forma indicada después de 150 días en un ensayo clínico, y la Figura 2 demuestra que la no adherencia no sólo provoca episodios temporales de toxicidad (por consumir dosis dobles) y falta de eficacia (omisión de dosis), sino que introduce variabilidad en los datos.
El aumento en la variabilidad de los datos provoca que los equipos responsables del estudio tengan que inscribir a más pacientes para lograr los resultados estadísticos establecidos. Es importante enfatizar que los incrementos lineales en la no adherencia tienen un impacto exponencial en el número de pacientes necesarios para obtener el mismo resultado estadístico. Es decir, una tasa de no adherencia de 20% -30% requiere un aumento del tamaño de la muestra del estudio del 50%, para mantener un poder estadístico equivalente; cuando la no adherencia alcanza el 50%, el tamaño de la muestra debe aumentar en un 200% para mantener un poder estadístico equivalente [6]. Sin embargo, la discusión sobre el tema entre los profesionales de la industria sugiere que los científicos que diseñan el estudio no tienen en cuenta la posibilidad de no adherencia del paciente.
Impacto en los costos de la no adherencia al ensayo clínico
Hemos demostrado previamente que la falta de adherencia del paciente en los ensayos clínicos lleva a inscribir más pacientes para lograr los mismos resultados estadísticos, atrasa la finalización del ensayo y, posteriormente, eleva los costos de operación. En esta sección, estimaremos el costo de la no adherencia y el costo de oportunidad de reducir la no adherencia.
El Cuadro 2 modela los costos operacionales asociados con la no adherencia al producto experimental en los ensayos clínicos.
El Cuadro 2 indica que, en promedio, en todas las indicaciones terapéuticas, un ensayo de Fase III necesita inscribir a 460 pacientes adicionales (total de 828 pacientes) (Cuadro 1) para mantener un poder estadístico equivalente, asumiendo una tasa de no adherencia constante del 40%. El costo operacional para inscribir a 460 pacientes se calcula en US$12 millones. Al reducir la no adherencia en un 1% (al 39%), los patrocinadores necesitan inscribir a 13 pacientes menos para mantener un poder estadístico equivalente, resultando en ahorros de aproximadamente US$336.000 y, naturalmente, se minimiza el atraso en finalizar el ensayo.
Abordar la no adherencia
El análisis anterior muestra sólo un caso de no adherencia al estudio (no adherencia IMP), que tiene un impacto directo en la variabilidad de los datos y los resultados estadísticos. Cuando se combina con otras formas de no adherencia en los ensayos clínicos (es decir, abandono del sujeto, no completar cuestionarios de ePRO, ausencia de visitas de estudio y no seguir los procedimientos del estudio, etc.), la prolongación del estudio es inminente.
La cuestión de la no adherencia se puede abordar fácilmente con tecnologías novedosas. Por ejemplo, la Inteligencia Artificial (AI) ha avanzado hasta el punto de poderse convertir en compañero digital de los pacientes, les puede servir de guía a lo largo del ensayo clínico. Además, los nuevos modelos de diseño del estudio centrados en el paciente ahora están introduciendo maneras innovadoras de recopilar datos clínicos a través de Electronic Device Reported Outcomes (eDROs, por sus siglas en inglés), o que recopilan directamente de los pacientes a través de tecnología que lleva el paciente (wearables) y mHealth.
En el futuro, es probable que las tecnologías avanzadas y el diseño del estudio centrándose en el paciente no sólo haga que los estudios sean más convenientes y accesibles para los pacientes, sino que también mejore el cumplimiento de los pacientes con los procedimientos del estudio y el consumo del medicamento, generando mejor calidad de datos, acortando la duración del tratamiento y minimizando el impacto en los costos.
Moe Alsumidaie, MBA, MSF es Jefe de Ciencias de la Información en el Anexo Clínico, y miembro del Consejo Editorial Asesor y colaborador habitual de Applied Clinical Trials.
Referencias